题目内容
下列实验能成功的是( )
| A、将浓硫酸和乙醇混合加热140℃制乙烯 |
| B、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热,产生砖红色沉淀 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、苯和浓溴水反应制溴苯 |
考点:乙烯的实验室制法,苯的性质
专题:实验评价题
分析:A.实验室制备乙烯,温度应该控制在170℃,否则生成的是乙醚;
B.根据乙醛与新制的氢氧化铜浊液的反应现象进行判断;
C.CH3CH2Br没有自由移动的离子;
D.苯和溴水不反应.
B.根据乙醛与新制的氢氧化铜浊液的反应现象进行判断;
C.CH3CH2Br没有自由移动的离子;
D.苯和溴水不反应.
解答:
解:A.将乙醇与浓硫酸共热到170℃制备乙烯,140℃时生成的是乙醚,故A错误;
B.醛类能够与新制的氢氧化铜浊液反应生成红色沉淀,所以CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热可以观察到有红色沉淀产生,故B正确;
C.CH3CH2Br没有自由移动的离子,应向CH3CH2Br中先加入氢氧化钠,再加入硝酸酸化的硝酸银以检验溴元素,所以CH3CH2Br中滴加AgNO3溶液观察则不能实现判断卤代烃的类型,故C错误;
D.苯和液溴在催化剂作用下反应生成溴苯,苯和溴水不反应,故D错误;
故选B.
B.醛类能够与新制的氢氧化铜浊液反应生成红色沉淀,所以CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热可以观察到有红色沉淀产生,故B正确;
C.CH3CH2Br没有自由移动的离子,应向CH3CH2Br中先加入氢氧化钠,再加入硝酸酸化的硝酸银以检验溴元素,所以CH3CH2Br中滴加AgNO3溶液观察则不能实现判断卤代烃的类型,故C错误;
D.苯和液溴在催化剂作用下反应生成溴苯,苯和溴水不反应,故D错误;
故选B.
点评:本题以实验形成考查物质的性质,注意在解此类题时,首先需要知道物质发生反应的条件,熟记各官能团的性质是解题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学用语及其说法正确的是( )
| A、H、D、T互为同素异形体,化学性质几乎完全相同 |
B、硫离子结构示意图: |
| C、吸氧腐蚀的正极反应式为:O2+2H2O+4e-═4OH- |
D、NaOH的电子式为: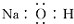 |
下列说法中不正确的是( )
| A、同系物的化学性质相似 |
| B、甲烷和环丙烷是同系物 |
| C、相对分子质量相同的几种化合物不一定互为同分异构体 |
| D、分子组成相差若干个CH2原子团的有机物不一定是同系物 |
某强酸性溶液X中还可能含有Fe2+、Al3+、NH4+、AlO2-、CO32-、SO42-,SiO32-、Cl-、H2SO3中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法上正确的是( )

下列说法上正确的是( )
| A、由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有Fe2+ |
| B、由实验②可知,气体D一定是NH3,原溶液中肯定含有NH4+,肯定不含Al3+ |
| C、由实验③可知,沉淀G可能是Al(OH)3和BaCO3 |
| D、原溶液中肯定含有Al3+,NH4+、H2SO3不能确定是否含有SO42- |
下列变化属于氧化还原反应的是( )
| A、BaCl2+Na2S04═BaS04↓+2NaCl | ||||
B、2H2+02
| ||||
C、NH4HC03
| ||||
D、CaC03
|
通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
| A、分子中的所有原子均达到8电子稳定结构 |
| B、分子中N-C1键键长与CCl4分子中C-Cl键键长相等 |
| C、NCl3分子是平面三角形非极性分子 |
| D、NBr3比NCl3易挥发 |
下列各组化合物的晶体都属于分子晶体的是( )
| A、H2O,O3,NaCl |
| B、CCl4,(NH4)2S,H2O2 |
| C、SO2,SiO2,CS2 |
| D、P2O5,CO2,H3PO4 |
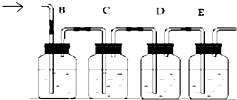 实验室用乙醇和浓硫酸加热反应制取乙烯,其原理为:
实验室用乙醇和浓硫酸加热反应制取乙烯,其原理为: