题目内容
【题目】电解NaB(OH)4溶液制备H3BO3的原理如图所示,下列叙述错误的是( )

A. M室发生的电极反应式:2H2O﹣4e﹣=O2↑+4H+
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N室中:a%<b%
D. 每生成1mol H3BO3,则有1mol Na+进入N室
【答案】B
【解析】
该装置有外加电源,因此该装置电解池,左端石墨为阳极,根据电解原理,阳极反应式为2H2O-4e-=O2↑+4H+,产品室得到产品,因此a膜为阳离子交换膜,右端石墨为阴极,根据电解原理,阴极反应式为2H2O+2e-=H2↑+2OH-,c膜为阳离子交换膜;
该装置有外加电源,因此该装置电解池,左端石墨为阳极,根据电解原理,阳极反应式为2H2O-4e-=O2↑+4H+,产品室得到产品,因此a膜为阳离子交换膜,右端石墨为阴极,根据电解原理,阴极反应式为2H2O+2e-=H2↑+2OH-,c膜为阳离子交换膜;
A、M室中石墨电极为阳极,电解时阳极上水失电子生成O2和H+,电极反应式为2H2O﹣4e﹣═O2↑+4H+,故A说法正确;
B、原料室中的B(OH)4﹣通过b膜进入产品室,M室中氢离子通入a膜进入产品室,原料室中的Na+通过c膜进入N室,则a、c为阳离子交换膜,b为阴离子交换膜,故B说法错误;
C、N室中石墨为阴极,电解时阴极上水得电子生成H2和OH﹣,原料室中的钠离子通过c膜进入N室,溶液中c(NaOH)增大,所以N室:a%<b%,故C说法正确;
D、理论上每生成1molH3BO3,则M室中就有1mol氢离子通入a膜进入产品室即转移1mole﹣,原料室中的1molNa+通过c膜进入N室,故D说法正确。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】市售一次性电池品种很多的,碱性锌锰电池的日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
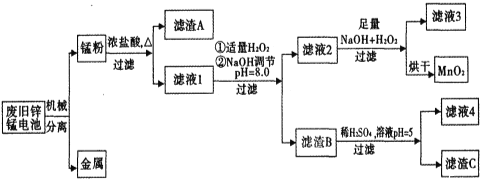
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含量有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表。
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2/Mn(OH)3 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH (c≤1.0x10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是___。计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=___。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式___。
(3)写出滤渣B与稀硫酸在pH=5时的化学方程式___。
(4)工艺中还可以将滤液4进行___、___、___、___、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4,在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式___。
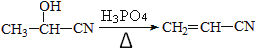
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的是有机液体,可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂瓶中所装液体的名称。已知:乙酸乙酯在稀![]() 溶液中发生水解反应的化学方程式为
溶液中发生水解反应的化学方程式为![]() 。
。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
试写出下列标号代表的液体名称:
A_______,B_______,C_______,D_______,E_______,F_______,G_______。