题目内容
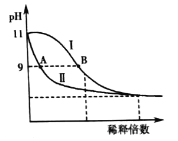
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请回答以下问题。
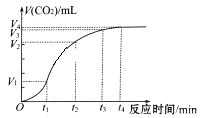
(1)化学反应速率最快的时间段是_________,原因是________________。
A.0~t1 B.t1-t2 C. t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸溶液中加入下列物质,你认为可行的有_________。
A.蒸馏水 B.NaCl固体
C.NaCl溶液 D.通入HCl
(3)若盐酸溶液的体积是20mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)=________________mol·L-1·min-1。
【答案】B 反应放热 AC (V2-V1)/[224x(t2-t1)]
【解析】
(1)从图中可以看出,化学反应速率最快的时间段是.t1-t2。答案为:.B
因为随着反应的进行,c(H+)不断减小,如果影响反应速率的因素只有c(H+),则反应速率应不断减慢,但.t1-t2段反应速率加快,说明还有其它因素影响反应速率,只能是温度,从而说明反应放热。,答案为:反应放热
(2)A.蒸馏水,稀释溶液,使c(H+)减小,反应速率减慢,A符合题意;
B.NaCl固体,不影响c(H+),溶液的温度也没有变化,所以对反应速率不产生影响,B不符合题意;
C.NaCl溶液,相当于加水稀释,c(H+)减小,反应速率减慢,C不合题意;
D.通入HCl,增大c(H+),加快反应速率,符合题意。
故选AC。
(3)若盐酸溶液的体积是20mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)=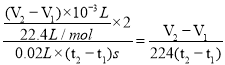 mol·L-1·min-1。
mol·L-1·min-1。
答案为:![]()

练习册系列答案
相关题目