题目内容
11.如果Mg2+、M、Fe3+、Cl-四种离子以物质的量之比1:2:2:4共存于同一溶液中,则M可能是( )| A. | SO${\;}_{4}^{2-}$ | B. | CO${\;}_{3}^{2-}$ | C. | OH- | D. | NO${\;}_{3}^{-}$ |
分析 任何电解质溶液中都呈电中性,根据电荷守恒判断M可能是哪种离子,这四种离子能共存,说明这四种离子之间不反应,据此分析解答.
解答 解:任何电解质溶液中都呈电中性,假设Mg2+、M、Fe3+、Cl-四种离子的物质的量分别是1mol、2mol、2mol、4mol,该溶液中2n(Mg2+)+3n(Fe3+)-n(Cl-)=2×1mol+3×2mol-4×1mol=4mol>0,要使溶液呈电中性,则M应该带负电荷,因为M的物质的量是2mol,则每个M带2个单位负电荷,但碳酸根和铁离子、镁离子不能构成,故选A.
点评 本题考查离子共存、物质的量的有关计算,侧重考查学生分析判断能力,明确溶液中存在电荷守恒是解本题关键,还要考虑离子共存问题,为易错点.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
1.下列关于乙烯的说法正确的是( )
| A. | 是天然气的主要成分 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | 不能发生燃烧反应 | D. | 不能发生加聚反应 |
19.某无色溶液中,可大量共存的离子组是( )
| A. | Na+、HCO3-、SO42-、Br- | B. | Cu2+、NO3-、Cl-、SO42- | ||
| C. | H+、Cl-、Na+、CO32- | D. | H+、Na+、S2-、NO3- |
6.下列溶液中,氯离子浓度最大的是( )
| A. | 200mL 1mol•L-1 的NaCl溶液 | B. | 150mL 1mol•L-1 的MgCl2溶液 | ||
| C. | 100mL 1mol•L-1 的HCl溶液 | D. | 50mL 1mol•L-1 的AlCl3溶液 |
16.下列反应中,下面划线的元素被氧化的是( )
| A. | Cl2+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2 | |
| B. | SO2+2H2S═3S↓+2H2O | |
| C. | 8CuFeS2+21O2$\frac{\underline{\;高温\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2 | |
| D. | NH3+HNO3═NH4NO3 |
2.已知下列数据:
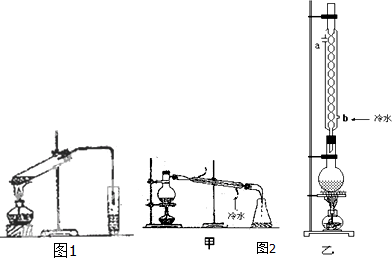
实验室制乙酸乙酯的主要装置如图1所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到15mL试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处,③小火加热试管中的混合液;④待小试管中收集约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯.
请同学们回答下列问题:
(1)写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,浓H2SO4的作用是催化剂、吸水剂.
(2)步骤④所观察到的现象是在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,原因是上层是油层因为生成的乙酸乙酯难溶于水,且密度比水小,同时因为挥发出来的乙酸与碳酸钠反应,放出CO2气体,所以有气泡出现.
(3)步骤⑤中,分离出乙酸乙酯选用的仪器是分液漏斗.
(4)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如图2甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物).你认为哪种装置合理,为什么?答:乙,反应物能冷凝回流.
| 物 质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 乙 醇 | -114 | 78 | 0.789 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |

实验室制乙酸乙酯的主要装置如图1所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到15mL试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处,③小火加热试管中的混合液;④待小试管中收集约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯.
请同学们回答下列问题:
(1)写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,浓H2SO4的作用是催化剂、吸水剂.
(2)步骤④所观察到的现象是在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,原因是上层是油层因为生成的乙酸乙酯难溶于水,且密度比水小,同时因为挥发出来的乙酸与碳酸钠反应,放出CO2气体,所以有气泡出现.
(3)步骤⑤中,分离出乙酸乙酯选用的仪器是分液漏斗.
(4)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如图2甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物).你认为哪种装置合理,为什么?答:乙,反应物能冷凝回流.
20.下列说法正确的是( )
| A. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| B. | 非标准状况下,1mol任何气体的体积不可能为22.4L | |
| C. | 标准状况下22.4L任何气体都含有约6.02×1023个分子 | |
| D. | 在标准状况下1mol H2O的体积约为22.4L |
