题目内容
【题目】最新发现的第113号、115号、117号和118号元素已正式写入元素周期表。根据物质结构、元素周期律的知识,下列说法正确的是( )
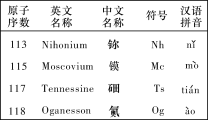
A. Nh(OH)3具有两性
B. Mc位于元素周期表中第七周期第ⅤA族,其原子半径小于Ts
C. Og是一种人工合成的稀有气体元素,在元素周期表中位于第七周期0族
D. 若制得Ts的最高价氧化物对应的水化物,其酸性强于HClO4
【答案】C
【解析】
根据元素周期表各周期元素种数从1~7周期依次为:2、8、8、18、18、32、32,不难推出,第113号、115号、117号和118号元素在元素周期表中的位置,然后根据同周期或同主族元素性质递变规律来解答。
A. Nh是113号元素,在周期表中位于第7周期第IIIA族,和Al位于同一主族,同一主族从上到下元素的金属性逐渐增强,最高价氧化物的水化物碱性逐渐增强,所以Nh(OH)3具有碱性,故A错误;
B. Mc是115号元素,位于元素周期表中第七周期第ⅤA族,Ts是117号元素,位于元素周期表中第七周期第VIIA族,同一周期元素原子半径从左到右逐渐减小,Mc原子半径大于Ts,故B错误;
C. Og是118号元素,位于元素周期表中第七周期第0族,一种人工合成的稀有气体元素,故C正确;
D. Ts是117号元素,位于元素周期表中第七周期第VIIA族,与Cl位于同一主族,同一主族从上到下,元素的非金属性逐渐减弱,其最高价氧化物对应的水化物酸性逐渐减弱,所以若制得Ts的最高价氧化物对应的水化物,其酸性弱于HClO4,故D错误。
故答案选C。

【题目】二氯化二硫(S2Cl2)是一种黄红色液体,有刺激性、窒息性恶臭。生产中使用它作橡胶的低温硫化剂和黏结剂。向熔融的硫中通入限量氯气即可生成S2Cl2,进一步氯化可得SCl2。S2Cl2、SCl2的某些性质如下表所示:
水溶性 | 密度(g/cm3) | 熔点 | 沸点 | |
S2Cl2 | 空气中发烟雾,遇水即水解 | 1.687 | -76 ℃ | 138 ℃ |
SCl2 | 溶于水且剧烈反应 | 1.621 | -122 ℃ | 59 ℃ |
实验室可用如图所示装置制备少量S2Cl2。请回答下列问题:
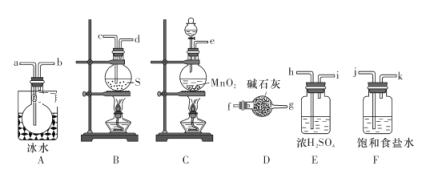
(1)已知S2Cl2分子中各原子最外层均满足8电子稳定结构,则S2Cl2的电子式为__________。
(2)从上图所示装置中选用某一装置制取Cl2,发生反应的离子方程式为__________。
(3)欲得到较纯净的S2Cl2,上述仪器装置的连接顺序为:
e→______→_____→______→______→______→______→a→b→______→_______(按气流方向填小写字母代号)。
(4)仪器D的名称是__________,D中碱石灰的作用是__________。
(5)为了获得更纯净的S2Cl2,需要对产品进行的操作是_______。
(6)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的化学方程式:__________;该反应中被氧化和被还原的元素的质量之比为______。