题目内容
1.如图为Zn、铜水果电池装置示意图,下列说法正确的是( )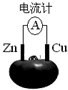
| A. | 铜片为负极,发生还原反应 | B. | 锌片上发生还原反应:Zn-2e-=Zn2+ | ||
| C. | 该装置将电能转变为化学能 | D. | 电子由锌片沿导线流向铜极 |
分析 根据金属的活泼性知,Zn作负极,Cu作正极,负极上Zn失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,据此解答.
解答 解:A、根据金属的活泼性知,Zn作负极,发生氧化反应,故A错误;
B、锌片上发生氧化反应:Zn-2e-=Zn2+,故B错误;
C、该装置能将化学能转化为电能,故C错误;
D、电子由负极Zn经导线流向正极Cu,故D正确;
故选D.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,难度不大,明确电子的移动方向、电极的判断是解题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
11.共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①Na2O2;②SiO2;③石墨;④金刚石;⑤CaH2;⑥白磷(P4),其中含有两种结合力的组合是( )
| A. | ①③⑤⑥ | B. | ①③⑥ | C. | ②④⑥ | D. | ①②③⑥ |
12.现有CH3COOH和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是( )
| A. | $\frac{1-a}{7}$ | B. | $\frac{3}{4}$a | C. | $\frac{6}{7}$(1-a) | D. | $\frac{12}{13}$(1-a) |
16.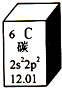 元素周期表是学习化学的重要工具.如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具.如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
 元素周期表是学习化学的重要工具.如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具.如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )| A. | 该元素的原子序数为6 | |
| B. | 该元素所有原子的质子数均为6 | |
| C. | 该元素的相对原子质量为12.01 | |
| D. | 该元素没有同位素,所有原子的中子数均为6 |
13.高温下,在容积固定的密闭容器中,用足量焦炭与一定量二氧化碳发生可逆的吸热反应生成了CO.下列选项中,一定符合反应达到化学平衡时情况的选项是( )
| A. | 压缩体积达到新平衡时,CO的浓度增大的倍数比CO2的浓度增大的倍数更大 | |
| B. | 速率关系:2v(CO2)=v(CO) | |
| C. | 转移电子数随温度升高而增多 | |
| D. | 气体密度随着焦炭的增加而增大 |
10.下列物质中,不属于醇类的是( )
| A. | C4H9OH | B. | C6H5CH2OH | C. | C6H5OH | D. | 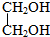 |
18. 在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )
在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )
 在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )
在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )| A. | 100% | B. | 56% | C. | 97.3% | D. | 93.8% |
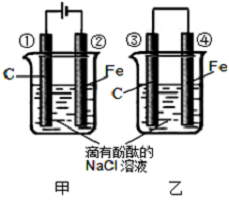 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.