题目内容
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
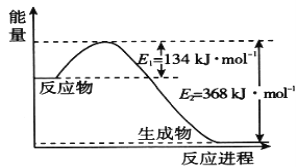
(1)如图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式 _________________________________________。
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数 K 与温度 T 的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数 K 与温度 T 的关系如下表:
T/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1 ______ K2(填“>”、“=” 或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_________(填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.3v正(N2) = v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应 2NH3(g) ![]() N2(g) + 3H2(g) 的平衡常数K为_________。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)______v逆(N2)(填“>”、“=” 或“<”)。
N2(g) + 3H2(g) 的平衡常数K为_________。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)______v逆(N2)(填“>”、“=” 或“<”)。
(3)在容积为2 L的密闭容器中,充入一定量CO2和H2合成甲醇(CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-58 kJ·mol1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
CH3OH(g)+H2O(g) ΔH=-58 kJ·mol1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
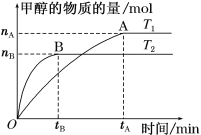
①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=______mol·L1·min1。
②图示的温度T1______T2(填“>”、“=” 或“<”)。
【答案】NO2(g)+CO(g)= NO(g)+CO2(g) ΔH=234 kJ mol1 > bc 2 > ![]() <
<
【解析】
(1)根据能量变化图,反应热等于正反应的活化能减去逆反应的活化能;
(2)①对于放热反应,温度越高,平衡逆向移动,反应平衡常数越小;
②根据平衡状态的判断依据判断;
③400℃时,N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数 K =0.5,反应 2NH3(g)
2NH3(g) ΔH<0,其化学平衡常数 K =0.5,反应 2NH3(g) ![]() N2(g) + 3H2(g) 的平衡常数K为
N2(g) + 3H2(g) 的平衡常数K为![]() =2;
=2;
根据浓度熵和平衡常数的关系来确定平衡的移动方向;
(3)①结合v=△c÷△t计算;
②由图T2先达到平衡,温度高,速度快,图示的温度T1<T2。
(1)该反应的焓变△H=E1-E2=134KJ·mol-1-368KJ·mol-1=-234KJ·mol-1,所以热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ·mol-1;
(2)①该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,生成物浓度减小,反应物浓度增大,所以K1>K2;
②a、容器内各物质的浓度之比等于计量数之比,不能证明正逆反应速率相等,故a错误;
b、不同物质的正逆反应速率之比等于其计量数之比是平衡状态,3v正(N2) = v逆(H2)
是平衡状态,故b正确;
c、容器内压强不变,气体的物质的量不变,该反应达平衡状态,故c正确;
d、如果是在密闭容器中反应,质量不变,体积不变,密度始终不变,故d错误;
故选bc;
③400℃时,N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数 K =0.5,反应 2NH3(g)
2NH3(g) ΔH<0,其化学平衡常数 K =0.5,反应 2NH3(g) ![]() N2(g) + 3H2(g) 的平衡常数K为
N2(g) + 3H2(g) 的平衡常数K为![]() =2;
=2;
,400℃时,浓度商Qc=2×13÷32=<K,说明反应正向进行,因此有v正(N2)>v逆(N2);
(3)①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=△c÷△t=![]() ==
== ![]() mol·L1·min1。
mol·L1·min1。
②由图T2先达到平衡,温度高,速度快,图示的温度T1<T2。

【题目】Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.8×10﹣31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于_____(填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因__________________________。
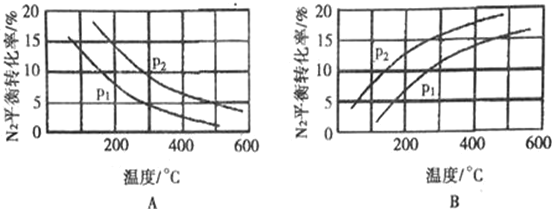
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是___(填“A”或“B”);比较P1、P2的大小关系:P1______P2(填“>”、“=” 或“<”)。
Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。达平衡时,H2的转化率α1=____。
【题目】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期律的重要性。下表列出了a~j10种元素在周期表中的位置:
周期 | IA | 0 | |||||||
1 | a | IIA | … | IIIA | IVA | VA | VIA | VIIA | |
2 | b | … | e | d | |||||
3 | c | f | … | g | h | i | j |
(1)因在元素b的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,b原子结构示意图为____;此类电池工作时,将___能转化为电能。
(2)a~j10种元素中,最外层电子数比K层电子数多的元素有___种(填数字);金属性最强的元素有_____(写元素符号)。
(3)元素g的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为:_______;
(4)h、i、j三种元素的气态氢化物中,最稳定的氢化物是______(写化学式);
(5)元素i的一种氧化物常用于漂白纸浆、草帽辫等。该氧化物具有还原性,在一定条件下能与常见氧化剂发生反应,写出其中一个反应的化学方程式:_______ 。