题目内容
(14分)研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802 kJ·mol-1
则CH4(g)+CO2(g) 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1
(2)在密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应
CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。

①据图可知,p1、p2、 p3、p4由大到小的顺序 。
②在压强为p4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为 。该温度下,反应的平衡常数为 。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g) CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。
① 在恒温恒容下,如果从反应物出发建立平衡,可认定平衡已达到的是
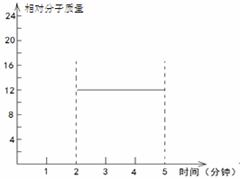
② 在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向 (填“正”或“逆”)反应方向移动,第5min时达到新的平衡,请在右图中画出2~5min内容器中气体平均相对分子质量的变化曲线。

(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802 kJ·mol-1
则CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1(2)在密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应
CH4(g)+CO2(g)
 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
①据图可知,p1、p2、 p3、p4由大到小的顺序 。
②在压强为p4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为 。该温度下,反应的平衡常数为 。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g)
 CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。① 在恒温恒容下,如果从反应物出发建立平衡,可认定平衡已达到的是
| A.体系压强不再变化 | B.H2与CO的物质的量之比为1:1 |
| C.混合气体的密度保持不变 | D.气体平均相对分子质量为15,且保持不变 |

(14分,每空2分)
(1) +248
(2) ①p4>p3>p2>p1
②0.032mol·L-1·min-1 1.64
(3) ① AC ② 逆 变化曲线见右图
(1) +248
(2) ①p4>p3>p2>p1
②0.032mol·L-1·min-1 1.64
(3) ① AC ② 逆 变化曲线见右图

试题分析:(1)已知
①2CO(g)+O2(g)=2CO2(g) △H1=-566 kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H2=-484 kJ·mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=-802 kJ·mol-1
根据盖斯定律,③-②-①得:CH4(g)+CO2(g)
 2CO(g)+2H2(g),故△H=△H3-△H2-△H1=-802 kJ·mol-1+484 kJ·mol-1+566 kJ·mol-1=+248kJ·mol-1。(2)①反应CH4(g)+CO2(g)
2CO(g)+2H2(g),故△H=△H3-△H2-△H1=-802 kJ·mol-1+484 kJ·mol-1+566 kJ·mol-1=+248kJ·mol-1。(2)①反应CH4(g)+CO2(g) 2CO(g)+2H2(g)为气体分子数增加的反应,当温度一定时,减小压强,可增大CH4的转化率,从图像可知,相同温度下,按p4、p3、p2、p1的顺序CH4的转化率增大,所以p4>p3>p2>p1。②根据X点CH4的转化率求得各物质的平衡浓度分别为:c(CH4)= c(CO2)=0.02mol·L-1,c(CO)= c(H2)=0.16mol·L-1,
2CO(g)+2H2(g)为气体分子数增加的反应,当温度一定时,减小压强,可增大CH4的转化率,从图像可知,相同温度下,按p4、p3、p2、p1的顺序CH4的转化率增大,所以p4>p3>p2>p1。②根据X点CH4的转化率求得各物质的平衡浓度分别为:c(CH4)= c(CO2)=0.02mol·L-1,c(CO)= c(H2)=0.16mol·L-1,故v (CO) =
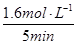 = 0.032mol·L-1·min-1;K =
= 0.032mol·L-1·min-1;K = 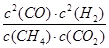 =
= 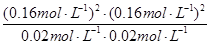 = 1.64(mol·L-1)2(通常不必写单位)。(3)①A项,恒容条件下,随着反应的进行,气体的物质的量增加,压强增大,若体系压强不变,说明达到了平衡状态;B项,从反应物出发建立平衡,则生成的CO和H2的物质的量总是相等的,所以当H2与CO的物质的量之比为1:1时不能确定是否达到平衡状态;C项,随着反应的进行,气体的质量增加,而体积不变,所以密度增大,当气体密度不变时,可以认定达到了平衡状态;D项,只有当反应完全生成CO和H2时,气体平均相对分子质量才能等于15,但一定条件下的可逆反应是不能进行完全的,所以不会出现D项所描述的状态。②加压时,平衡向着气体分子数减小的方向即逆反应方向移动;平衡气体的平均相对分子质量为M =
= 1.64(mol·L-1)2(通常不必写单位)。(3)①A项,恒容条件下,随着反应的进行,气体的物质的量增加,压强增大,若体系压强不变,说明达到了平衡状态;B项,从反应物出发建立平衡,则生成的CO和H2的物质的量总是相等的,所以当H2与CO的物质的量之比为1:1时不能确定是否达到平衡状态;C项,随着反应的进行,气体的质量增加,而体积不变,所以密度增大,当气体密度不变时,可以认定达到了平衡状态;D项,只有当反应完全生成CO和H2时,气体平均相对分子质量才能等于15,但一定条件下的可逆反应是不能进行完全的,所以不会出现D项所描述的状态。②加压时,平衡向着气体分子数减小的方向即逆反应方向移动;平衡气体的平均相对分子质量为M = 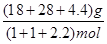 = 12g·mol-1,从化学方程式可看出,当正(逆)向平衡移动时,气体的质量变化增加(减少)12g,而气体的物质的量相应增加(减少)1mol,所以混合气体的相对分子质量并不发生变化,即M恒定为12g·mol-1。
= 12g·mol-1,从化学方程式可看出,当正(逆)向平衡移动时,气体的质量变化增加(减少)12g,而气体的物质的量相应增加(减少)1mol,所以混合气体的相对分子质量并不发生变化,即M恒定为12g·mol-1。
练习册系列答案
相关题目
 2SO3(g) ΔH<0
2SO3(g) ΔH<0
 AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应: 4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。
4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。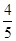 v(NH3)=v(O2)
v(NH3)=v(O2) 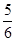 v(O2)=v(H2O)
v(O2)=v(H2O)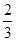 v(NH3)=v(H2O)
v(NH3)=v(H2O)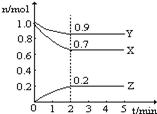
 ?2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
?2NH3(g) ΔH<0,反应过程如图:下列说法正确的是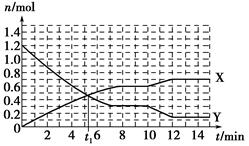
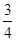 mol·L-1·min-1
mol·L-1·min-1 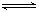 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是