题目内容
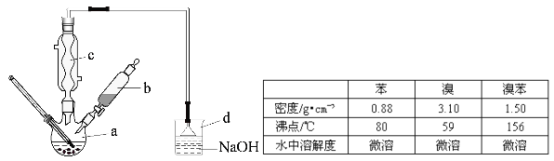
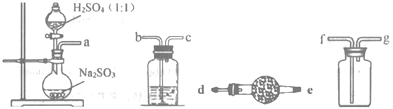
【题目】I.取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:①滴加适量H2O2,紫红色褪去,并有气泡产生;②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色; ③最后通入足量的SO2气体。请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为________;
(2)实验③中的现象为_____;
(3)实验①中反应的离子方程式是_________________。
(4)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为___。
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
Ⅱ.某工业废水中仅含表中的离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
阳离子 | K+、Cu2+、Fe3+、 Al3+、Fe2+ |
阴离子 |
|
甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
②取少量溶液,加入KSCN溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)③中加入少量盐酸生成无色气体的离子方程式是____________________。
(2)将③中红棕色气体(标况下)收集满一试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为___________mol/L(精确到千分位)。
(3)甲同学最终确定原溶液中所含离子是__________________。
【答案】PbO2>KMnO4>H2O2 溶液紫红色褪去,有白色沉淀生成 2MnO4—+5H2O2+6H+=2Mn2++5O2↑+8H2O C 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O 0.045 Fe2+、Cu2+ Cl-、NO3-、SO42-
【解析】
I.(1)实验①说明H2O2能被KMnO4氧化,所以氧化性:KMnO4>H2O2;实验②说明Mn2+能与PbO2反应生成KMnO4,得出氧化性:PbO2>KMnO4,综上得出,氧化性顺序是:PbO2>KMnO4>H2O2,故答案为:PbO2>KMnO4>H2O2;
(2)实验③中SO2还原性较强,能使酸性KMnO4褪色,SO2被氧化为H2SO4,H2SO4和Pb2+反应生成PbSO4白色沉淀,故答案为:溶液紫红色褪去,有白色沉淀生成;
(3)实验①是H2O2被KMnO4氧化生成氧气以及锰离子的过程,即2MnO42-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故答案为:2MnO2+5H2O2+6H+═2Mn2++5O2↑+8H2O;
(4)证明某溶液中不含Fe3+而可能含有Fe2+,先加KSCN溶液无现象,排除铁离子,再加氯水观察是否为血红色,实验操作时的最佳顺序为③加少量KSCN溶液、①加入足量氯水,若溶液先无现象,后为血红色,则含亚铁离子,故答案为:C;
Ⅱ.①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察),说明没有K+;
②取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+;
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变,说明 Fe2+与NO3-和H+反应生成NO,即溶液中有Fe2+、NO3-,加盐酸溶液中阴离子种类不变,说明原溶液中有Cl-,加盐酸溶液依然澄清,说明没有SiO32-;
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成,说明有SO42-;
(1)③中加入少量盐酸生成无色气体,是Fe2+与NO3-和H+反应生成NO,其离子方程式:3Fe2++NO3-+4H+═3Fe3++NO+2H2O,故答案为:3Fe2++NO3-+4H+═3Fe3++NO+2H2O;
(2)标准状况下,将一充满NO2气体的试管,倒扣于水中,3NO2 + H2O =2HNO3 + NO,至液面不再升高时,得到硝酸溶液,设试管体积为VL,最终试管中所得溶液的浓度为 =0.045mol/L,故答案为:0.045;
=0.045mol/L,故答案为:0.045;
(3)由以上推断可知溶液中阴离子为 Cl-、NO3-、SO42-,且各为0.1mol/L,已经推断出的阳离子是Fe2+,其浓度为0.1mol/L,由电荷守恒可知溶液中还有一种+2价阳离子,所以还有Cu2+,所以甲同学最终确定原溶液中所含阳离子是:Fe2+、Cu2+;阴离子是:Cl-、NO3-、SO42-,故答案为:Fe2+、Cu2+;Cl-、NO3-、SO42-。

 名校课堂系列答案
名校课堂系列答案【题目】Q、W、X、Y、Z都是短周期主族元素,X、Y、Q在周期表中的位置关系如图所示,W、Z的最外层电子数相同,Z的核电荷数是W的2倍,则下列说法不正确的是( )
ⅠA | ⅡA | ⅢA | ⅣA |
Q | |||
X | Y |
A.非金属性:![]()
B.原子半径:![]()
C.最高价氧化物对应水化物的碱性:![]()
D.最简单氢化物的稳定性:![]()
【题目】已知25 ℃时有关弱酸的电离平衡常数见下表:
弱酸化学式 | HA | H2B |
电离平衡常数(25 ℃) | Ka=1.7×10-6 | Ka1=1.3×10-3 Ka2=5.6×10-8 |
则下列有关说法正确的是( )
A.NaHB溶液中部分微粒浓度的大小为:c(Na+)>c(HB-)>c(B2-)>c(H2B)
B.等物质的量浓度的各溶液pH关系为:pH(Na2B)>pH(NaHB)>pH(NaA)
C.向Na2B溶液中加入足量的HA溶液发生反应的离子方程式为:B2-+2HA=2A-+H2B
D.将a mol/L的HA溶液与a mol/L的NaA溶液等体积混合,混合液中:c(Na+)>c(A-)
【题目】有![]() 、
、![]() 、
、![]() 三种晶体,分别由
三种晶体,分别由![]() 、
、![]() 、
、![]() 、
、![]() 四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。
四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。
晶体 | 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与 |
| 801 | 较大 | 易溶 | 水溶液(或熔融)导电 | 白色沉淀 |
| 3500 | 很大 | 不溶 | 不导电 | 不反应 |
|
| 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(1)晶体的化学式分别为![]() ______;
______;![]() ______。
______。
(2)晶体的类型分别为![]() ______;
______;![]() ______,
______,![]() ______。
______。
(3)![]() 、
、![]() 晶体中粒子间的作用力分别为______、______。
晶体中粒子间的作用力分别为______、______。