题目内容
15.随着原子序数的递增,不呈周期性变化的是元素的( )| A. | 化合价 | B. | 相对原子质量 | ||
| C. | 原子的最外层电子排布 | D. | 原子半径 |
分析 随着原子序数的递增,核外电子排布、元素的化合价、原子半径、金属性和非金属性呈现周期性变化.
解答 解:随着原子序数的递增,核外电子排布、元素的化合价、原子半径、金属性和非金属性呈现周期性变化,但由于相对原子质量的决定因素是原子中质子数、中子数及同一元素的同位素原子在自然界中的物质的量分数,所以相对原子质量不呈周期性变化,
故选:B.
点评 本题考查随着原子序数的递增,元素性质的变化,要理解元素性质呈周期性变化的原因是元素原子的核外电子排布的周期性变化的结果.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.已知25℃时,醋酸、碳酸、次氯酸、氢氟酸和亚硫酸的电离平衡常数分别为
(1)写出H2SO3的电离方程式H2SO3?H++HSO3-,HSO3-?H++SO32-.
(2)在25℃时,相同物质量浓度、相同体积的上述五种酸溶液中,氢离子浓度最大的是H2SO3(填“醋酸”、“碳酸”、“次氯酸”、“氢氟酸”或“亚硫酸”,下同);水电离的氢离子浓度最大的是HClO.
(3)在25℃时,0.1mol•L-1的氢氟酸的电离度=6%;溶液pH的测定可用广泛pH试纸,其操作方法是:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有HF溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较,确定溶液的pH;加水稀释该氢氟酸溶液,下列数值增大的是BD.
A.c(F-) B.c(OH-) C.c(H+)•c(OH-) D.c(F-)/c(HF) E.c(F-)/c(HF)•c(OH-)
(4)下列离子方程式中正确的是AC.
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-═HCO3-+HClO
B.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
C.过量SO2通入碳酸钠溶液中:2SO2+H2O+CO32-═2HSO3-+CO2
D.过量CH3COOH加入碳酸钠溶液中:CH3COOH+CO32-═CH3COO-+HCO3-
(5)若反应反应:Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,可以加入E.
A.Na2SO3 B.H2O C.Na2CO3D.NH3•H2OE.NaHCO3
(6)常温下,0.1mol/L醋酸溶液与0.01mol/L醋酸溶液中的c(H+)分别为A与B,则两者的c(H+)大小关系为:A小于10B.(填“大于”、“等于”、“小于”)
| 弱电解质 | CH3COOH | HClO | HF | H2CO3 | H2SO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka=3.6×10-4 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.5×10-2 Ka2=1.0×10-7 |
(2)在25℃时,相同物质量浓度、相同体积的上述五种酸溶液中,氢离子浓度最大的是H2SO3(填“醋酸”、“碳酸”、“次氯酸”、“氢氟酸”或“亚硫酸”,下同);水电离的氢离子浓度最大的是HClO.
(3)在25℃时,0.1mol•L-1的氢氟酸的电离度=6%;溶液pH的测定可用广泛pH试纸,其操作方法是:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有HF溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较,确定溶液的pH;加水稀释该氢氟酸溶液,下列数值增大的是BD.
A.c(F-) B.c(OH-) C.c(H+)•c(OH-) D.c(F-)/c(HF) E.c(F-)/c(HF)•c(OH-)
(4)下列离子方程式中正确的是AC.
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-═HCO3-+HClO
B.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
C.过量SO2通入碳酸钠溶液中:2SO2+H2O+CO32-═2HSO3-+CO2
D.过量CH3COOH加入碳酸钠溶液中:CH3COOH+CO32-═CH3COO-+HCO3-
(5)若反应反应:Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,可以加入E.
A.Na2SO3 B.H2O C.Na2CO3D.NH3•H2OE.NaHCO3
(6)常温下,0.1mol/L醋酸溶液与0.01mol/L醋酸溶液中的c(H+)分别为A与B,则两者的c(H+)大小关系为:A小于10B.(填“大于”、“等于”、“小于”)
10.下列说法不正确的是( )
| A. | 由反应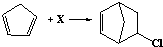 可知,X为氯乙烯 可知,X为氯乙烯 | |
| B. | 异辛烷的结构为(CH3)3CCH2CH(CH3)2,它的一氯代物共有4种同分异构体(不考虑对映异构体),且它们的熔点、沸点各不相同 | |
| C. | 已知CHCl3+HF→CHFCl2+HCl,此反应与由苯制备溴苯的反应类型相同 | |
| D. | 棉、毛、丝、麻完全燃烧时,都只生成CO2和H2O |
20.在强碱溶液中,可能大量存在的离子组是( )
| A. | Na+、K+、AlO2-、Cl- | B. | Ba2+、Na+、Al3+、SO42- | ||
| C. | K+、Mg2+、Cl-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
7.某同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A. | 所用NaOH已经潮解 | |
| B. | 向容量瓶中加水定容时俯视标线 | |
| C. | 用量筒量取所需的浓盐酸时俯视刻度线 | |
| D. | 定容后倒转容量瓶几次,发现液面最低点低于标线,再补几滴水 |