题目内容
【题目】亚氯酸钠![]() 是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出
是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出![]() ,
,![]() 有类似
有类似![]() 的性质。某兴趣小组探究亚氯酸钠的制备与性质。
的性质。某兴趣小组探究亚氯酸钠的制备与性质。
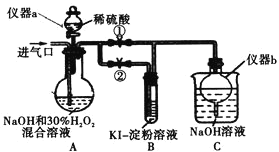
(I)制备亚氯酸钠
关闭止水夹![]() ,打开止水夹
,打开止水夹![]() ,从进气口通入足量
,从进气口通入足量![]() ,充分反应。
,充分反应。
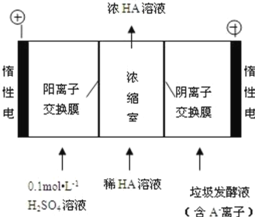
(1)仪器a的名称为_________,仪器b的作用是_________。
(2)装置A中生成![]() 的化学方程式为_________。
的化学方程式为_________。
(3)若从装置A反应后的溶液中获得![]() 晶体,则主要操作有:减压蒸发浓缩、________、过滤、洗涤、干燥等。
晶体,则主要操作有:减压蒸发浓缩、________、过滤、洗涤、干燥等。
(II)探究亚氯酸钠的性质
停止通![]() 气体,再通入空气一段时间后,关闭止水夹
气体,再通入空气一段时间后,关闭止水夹![]() ,打开止水夹
,打开止水夹![]() ,向A中滴入稀硫酸。
,向A中滴入稀硫酸。
(4)请写出这时A中发生反应的离子方程式_________。
(5)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因_________。
(6)B中现象为_________。
【答案】分液漏斗 防止倒吸 ![]() 降温结晶
降温结晶![]() 或冷却结晶
或冷却结晶![]()
![]()
![]() 与
与![]() 反应生成的
反应生成的![]() 对反应起催化作用 溶液变蓝色
对反应起催化作用 溶液变蓝色
【解析】
![]() 根据装置图判断仪器a的名称;仪器b是球形干燥管,可以防止发生倒吸;
根据装置图判断仪器a的名称;仪器b是球形干燥管,可以防止发生倒吸;
![]() 二氧化氯在碱性溶液中与过氧化氢反应生成亚氯酸钠、水和氧气;
二氧化氯在碱性溶液中与过氧化氢反应生成亚氯酸钠、水和氧气;
![]() 根据从溶液中获得晶体的基本操作回答;
根据从溶液中获得晶体的基本操作回答;
![]() 在酸性条件下生成NaCl并放出ClO
在酸性条件下生成NaCl并放出ClO![]() 气体;
气体;
![]() 根据影响反应速率的因素分析;
根据影响反应速率的因素分析;
![]() 有类似
有类似![]() 的性质,所以在B装置中
的性质,所以在B装置中![]() 与KI发生反应生成碘单质。
与KI发生反应生成碘单质。
![]() 由仪器a的结构可知名称为分液漏斗;ClO
由仪器a的结构可知名称为分液漏斗;ClO![]() 有类似Cl
有类似Cl![]() 的性质,能与氢氧化钠溶液发生反应,仪器b的作用是防止发生倒吸;
的性质,能与氢氧化钠溶液发生反应,仪器b的作用是防止发生倒吸;
![]() 二氧化氯在碱性溶液中与过氧化氢反应生成亚氯酸钠、水和氧气,反应方程式为:
二氧化氯在碱性溶液中与过氧化氢反应生成亚氯酸钠、水和氧气,反应方程式为:![]() ;
;
![]() 从溶液中获得
从溶液中获得![]() 晶体,主要操作有减压蒸发浓缩、降温结晶
晶体,主要操作有减压蒸发浓缩、降温结晶![]() 或冷却结晶
或冷却结晶![]() 、过滤、洗涤、干燥等;
、过滤、洗涤、干燥等;
![]() 在酸性条件下生成NaCl并放出ClO
在酸性条件下生成NaCl并放出ClO![]() , A中发生反应的离子方程式为:
, A中发生反应的离子方程式为:![]() ;
;
![]() 开始时A中反应缓慢,稍后产生气体的速率急剧加快,可推知反应产生了催化剂,应为生成的
开始时A中反应缓慢,稍后产生气体的速率急剧加快,可推知反应产生了催化剂,应为生成的![]() 对反应起催化作用;
对反应起催化作用;
![]() 有类似
有类似![]() 的性质,所以在B装置中
的性质,所以在B装置中![]() 与KI发生反应生成碘单质,溶液变蓝色。
与KI发生反应生成碘单质,溶液变蓝色。

【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取9.0g A,升温使其汽化,测其密度是相同条件下氢气的45倍。 | (1)A的相对分子质量为:_____。 |
(2)将此9.0g A在足量纯氧气中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 | (2)A的分子式为:______。 |
(3)另取9.0g A,跟足量的碳酸氢钠粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L氢气(标准状况)。 | (3)写出A中含有的官能团:____、_____。 |
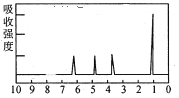
(4)A的核磁共振氢谱如图:
| (4)A中含有______种氢原子。 |
(5)综上所述A的结构简式__________。 | |