题目内容
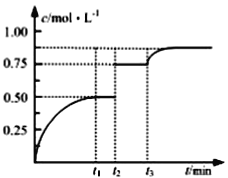
【题目】一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在t1时达到平衡:A(g)+B(g) ![]() xC(g)+D(s),在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s),在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
A. t1~t3间该反应的平衡常数相同,均为0.25 B. t2时刻改变的条件是使用催化剂
C. t3时刻改变的条件是移去少量物质D D. 反应方程式中x=2
【答案】D
【解析】试题分析:A、t1~t3间温度相同,平衡常数相同,由图可知平衡时C的浓度为0.5mol/L,则:
A(g)+B(g)2C(g)+D(s),
开始(mol/L):0.5 0.5 0
变化(mol/L):0.25 0.25 0.5
平衡(mol/L):0.25 0.25 0.5
所以平衡常数k=![]() =4,A错误;B、加入催化剂C的浓度不发生变化,B错误;C、D为固体,减少D的量,不影响平衡移动,C的浓度不发生变化,C错误;D、t2时刻C的浓度增大,浓度不变说明平衡不移动,应是增大压强造成的,压强不影响该平衡,所以有x=1+1=2,D正确;故选D。
=4,A错误;B、加入催化剂C的浓度不发生变化,B错误;C、D为固体,减少D的量,不影响平衡移动,C的浓度不发生变化,C错误;D、t2时刻C的浓度增大,浓度不变说明平衡不移动,应是增大压强造成的,压强不影响该平衡,所以有x=1+1=2,D正确;故选D。

【题目】已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
下列推断正确的是
A. 25℃时,同浓度的下列溶液 pH 关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
B. 若25℃时某溶液中c(CO32-)=c(HCO3-),则此溶液中 c(H+)=4.7×10-11 mol·L-1
C. 若某溶液中c(CO32-)=c(HCO3-),往该溶液中滴入盐酸, HCO3-比CO32-更易结合H+
D. 25℃时pH=9的CH3COONa和NaOH溶液,水电离出的c(H+)均为1×10-9mol·L-1
【题目】一定条件下,发生如下反应: A(s)+B(g)![]() C(s)+D(g)+E(g) △H<0,其中相对分子质量M(C)>M(A),起始时通入一定量的A 和B,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值。重新达到平衡后。纵坐标yY随X 变化趋势合理的是
C(s)+D(g)+E(g) △H<0,其中相对分子质量M(C)>M(A),起始时通入一定量的A 和B,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值。重新达到平衡后。纵坐标yY随X 变化趋势合理的是
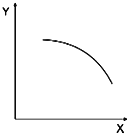
选项 | X | Y |
A | A的质量 | D的体积分数 |
B | B的物质的量 | B的转化率 |
C | B的浓度 | 平衡常数K |
D | 温度 | 容器内混合气体的平均摩尔质量 |
A. A B. B C. C D. D
【题目】活性炭可处理大气污染物NO.T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol | NO/mol | A/mol | B/mol | |
起始状态 | 2.030 | 0.100 | 0 | 0 |
2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2min内,用NO表示该反应的平均速率v(NO)=molL﹣1min﹣1 .
(2)该反应的化学方程式是 .
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是 .
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
①a处通入的物质是 , 电极反应式为:;
②b处电极反应式为;
③电池工作时H+由极移向极(填正、负极).