题目内容
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于一定体积密闭容器中的反应:N2(g)+3H2(g)![]() NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是()
NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是()

A. 点c处正反应速率比逆反应速率大 B. 点a的正反应速率比点b的正反应速率大
C. 气体的平均摩尔质量:点b大于点a D. 混合气体的密度:点b大于点a
【答案】D
【解析】A、点c处只能说明此时n(H2)=n(NH3),反应没有达到平衡,还在向正方向进行,故点c处正反应速率比逆反应速率大,选项A正确;B、从图象看出,在达到平衡的过程中,H2的物质的量不断减小,NH3的物质的量不断增大,所以此反应为向合成氨方向的反应,选项B正确;C、点a反应物的总物质的量比点b的大,总质量相同,故气体的平均摩尔质量: 点b大于点a,选项C正确;D、反应容器体积不变,气体总质量相同,故混合气体的密度:点b等于点a,选项D不正确。答案选D。

【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如表(KMnO4溶液用稀硫酸酸化),实验装置如图1:

实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.0lmol·L-1KMnO4溶液 |
② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |
(1)该反应的化学方程式为__________。
(2)该实验探究的是__________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积
大小关系是__________ < __________ (填实验序号)。
(3)若实验①在2min末收集了 2.24mLCO2 (标准状况下),则在2min末,c(MnO4-) =__________ mol·L-1。(假设混合溶液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定__________来比较化学反应速率。(一条即可)
(5)小组同学发现反应速率随时间的变化如图2所示,其中t1t2时间内速率变快的主要原因可能是:
①__________ ; ②__________ 。
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(S)+CO(g)![]() MgO(S)+CO2(g)+SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(S)+CO2(g)+SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )

选项 | x | y |
A | SO2的浓度 | 平衡常数K |
B | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
D | MgSO4的质量(忽略体积) | CO的转化率 |
A. A B. B C. C D. D
【题目】某研究小组将一批电子废弃物简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计如下制备硫酸铜晶体和无水氯化铁的方案:
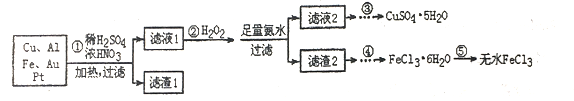
已知:Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O
请回答下列问题:
(1)步骤①Cu与酸反应的离子方程式为_________________________。
(2)步骤②加H2O2的作用是______________,滤渣2为(填化学式)__________。
(3)步骤⑤不能直接加热脱水的理由是________
(4)若滤液1中Cu2+的浓度为0.02mol·L-1,则氢氧化铜开始沉淀时的pH=________(已知:Ksp[Cu(OH)2]=2.0x10-20)
(5)已知:2Cu2++4I-=2CuI↓+I2 I2+2S2O32-=2I-+S4O62-
某同学为了测定CuSO4·5H2O产品的质量分数可按如下方法:取3.00g产品,用水溶解后,加入足量的KI溶液,充分反应后过滤、洗涤,将滤液稀释至250mL,取50mL加入淀粉溶液作指示剂,用0.080mol·L-1Na2S2O3标准溶液滴定,达到滴定终点的依据是______________。
四次平行实验耗去Na2S2O3标准溶液数据如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
此产品中CuSO4·5H2O的质量分数为__________。