题目内容
【题目】H2C2O4是一种二元弱酸,H2C2O4溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的H2C2O4溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
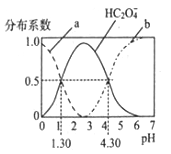
A. 曲线a代表H2C2O4,曲线b代表C2O42-
B. 常温下0.1mol/L的NaHC2O4溶液显酸性
C. 常温下,H2C2O4的电离平衡常数Ka2=10-4..30
D. pH从1.30~4.30时,  先增大后减小
先增大后减小
【答案】D
【解析】A.随着pH升高草酸分子的浓度逐渐减小,草酸氢跟离子的浓度逐渐增大,继续升高pH,草酸氢跟离子的浓度又逐渐减小,而草酸根离子的浓度开始逐渐增大,因此曲线a代表H2C2O4,曲线b代表C2O42-,A正确;B.根据图像可知当草酸氢跟离子浓度达到最大值时,溶液显酸性,所以常温下0.1mol/L的NaHC2O4溶液显酸性,B正确;C.根据图像可知当草酸氢跟和草酸根离子浓度相等时pH=4.3,所以草酸的第二步电离平衡常数Ka2=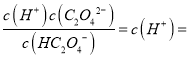 10-4.30,C正确;D.根据图像可知 pH从1.30~4.30时,
10-4.30,C正确;D.根据图像可知 pH从1.30~4.30时, 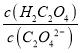 始终增大,D错误;答案选D。
始终增大,D错误;答案选D。

练习册系列答案
相关题目