题目内容
13.以下实验能获得成功的是( )| A. | 用酸性KMnO4溶液鉴别乙烯和乙炔 | |
| B. | 检验C2H5Cl中氯原子时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化 | |
| C. | 酒精与稀硫酸加热到170℃制乙烯 | |
| D. | 制取溴苯应用液溴、铁屑和苯混合,反应后并用稀碱液洗涤 |
分析 A.乙烯和乙炔均含不饱和键;
B.C2H5Cl和NaOH溶液混合加热后,发生水解反应,检验氯离子选择硝酸酸化;
C.稀硫酸不具有脱水性;
D.液溴和苯在铁屑作催化剂条件下发生取代反应,溴苯与碱液不反应,溴溶于碱液.
解答 解:A.乙烯和乙炔均能使酸性高锰酸钾溶液褪色,现象相同,不能鉴别,故A不选;
B.C2H5Cl和NaOH溶液混合加热后,发生水解反应,检验氯离子选择硝酸酸化,硫酸银、氯化银均为白色沉淀,则不能用稀硫酸酸化,故B不选;
C.稀硫酸不具有脱水性,则利用酒精与浓硫酸加热到170℃制乙烯,浓硫酸作催化剂、脱水剂,故C不选;
D.液溴和苯在铁屑作催化剂条件下发生取代反应,溴苯与碱液不反应,溴溶于碱液,则反应后并用稀碱液洗涤可得到溴苯,故D选;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的鉴别、离子检验、有机物的制备等,把握物质的性质、有机物的制备实验为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案
相关题目
4.某气态烃1mol能与2mol HCl完全加成,加成后产物分子中的氢原子又可被6mol Cl2完全取代,则此气态烃可能是( )
| A. | CH3C≡CCH3 | B. | CH2=CH2 | C. | CH≡CCH3 | D. | CH2=CHCH3 |
1.下列关于卤素的变化规律不正确的是( )
| A. | 单质的颜色逐渐加深 | B. | 气态氢化物的沸点:HCl>HBr>HI | ||
| C. | 酸性:HF<HCl<HBr<HI | D. | 酸性:HClO4>HBrO4>HIO4 |
8.以下各微粒中,所有原子都满足最外层为8电子结构的是( )
| A. | H3O+ | B. | BF3 | C. | CO2 | D. | PCl5 |
18.下列物质中,既能发生水解反应,又能发生加成反应,但不能发生消去反应的是( )
| A. | CH3-CH2-CH2-CH2Br | B. | CH2═CH-CH2-CH2-CH2Cl | ||
| C. | CH3Cl | D. | CH2═CH-CH2-C(CH3)2CH2Cl |
5.下列有关化学用语使用正确的是( )
| A. | 硫原子的原子结构示意图: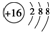 | |
| B. | 氚原子可表示为${\;}_{1}^{2}$H | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | 铁位于周期表第4周期第ⅧB族 |
2.2014年6月5日为世界环境日,主题为“提高你的呼声而不是海平面”,提倡节能减排,以下措施中不能体现这一思想的是( )
| A. | 提倡绿色生活,使用公共交通 | |
| B. | 大力发展火电,缓解用电紧张 | |
| C. | 开发太阳能、风能、氢能等清洁能源 | |
| D. | 研制出性能优良的催化剂,降低反应所需温度 |
3.原子序数为x的元素位于周期表中的第ⅡA族,则原子序数为x+1的元素不可能为( )
| A. | 第ⅢA族 | B. | 第ⅠA族 | C. | 镧系元素 | D. | 第ⅢB族 |