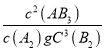题目内容
【题目】如图所示,已知A元素的最低化合价为-3价,它的最高价氧化物含氧56.21%,原子核内中子数比质子数多1,试回答(均用具体的元素符号或化学式回答):
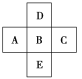
(1)写出它们的元素符号:A________,B________,C________,D________。
(2)A、B、C、D的气态氢化物稳定性最差的是________。
(3)A、B、C的原子半径由小到大的顺序是________。
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是_____________。
【答案】PSClOPH3Cl<S<PHClO4>H2SO4>H3PO4
【解析】
A元素的最低化合价为-3价,则其最高正价为+5价,最高价氧化物的化学式可表示为R2O5,设A元素的相对原子质量为Ar,则有: ![]() =56.21%,Ar≈31,即A为磷,B、C、D、E分别为硫、氯、氧、硒。(1)它们的元素符号分别为P、S、Cl、O。(2)根据元素周期律分析,A、B、C、D的气态氢化物稳定性最差的是PH3。(3)同周期元素,从左到右原子半径依次减小,故A、B、C的原子半径由小到大的顺序是Cl<S<P。(4)根据元素非金属性越强,其最高价氧化物对应的水化物的酸性越强分析,A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H3PO4。
=56.21%,Ar≈31,即A为磷,B、C、D、E分别为硫、氯、氧、硒。(1)它们的元素符号分别为P、S、Cl、O。(2)根据元素周期律分析,A、B、C、D的气态氢化物稳定性最差的是PH3。(3)同周期元素,从左到右原子半径依次减小,故A、B、C的原子半径由小到大的顺序是Cl<S<P。(4)根据元素非金属性越强,其最高价氧化物对应的水化物的酸性越强分析,A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H3PO4。

【题目】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g)![]() 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时AB3的反应速率/mol·L-1·min-1 | V甲 | v乙 | v丙 |
下列说法正确的是( )
A. K乙<K丙 B. c乙=c丙 C. a甲 +a乙<1 D. v甲=v丙
【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1。E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同。

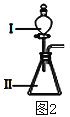
试回答:
(1)元素E在元素周期表中的位置是___________________。
(2)与元素D离子所含电子数和质子数均相同的微粒是________________。(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的_________________。若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:Ⅰ___________,Ⅱ__________,观察到的实验现象是________________________。
(4)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有___________________________________;
②b与c反应的化学方程式为_________________________________。