题目内容
18.有A、B、C三种烃,分别与H2加成反应后得到相同产物D.A、B、C各7g分别能与0.2g H2发生加成.则A、B、C名称依次是3-甲基-1-丁烯、2-甲基-2-丁烯、2-甲基-1-丁烯.分析 烃A、B、C各7g分别能与0.2g H2发生加成得到相同产物D,可知A、B、C为同分异构体,氢气为0.1mol,假设为烯烃,则A、B、C的物质的量为0.1mol,相对分子质量为$\frac{7}{0.1}$=70,组成通式为CnH2n,故14n=70,则n=5,烃的分子式为C5H10,由于戊烯有2种,故三种烯烃为CH2=CHCH(CH3)2,CH3CH=C(CH3)2,CH3CH2C(CH3)=CH2.
解答 解:烃A、B、C各7g分别能与0.2g H2发生加成得到相同产物D,可知A、B、C为同分异构体,氢气为0.1mol,假设为烯烃,则A、B、C的物质的量为0.1mol,相对分子质量为$\frac{7}{0.1}$=70,组成通式为CnH2n,故14n=70,则n=5,烃的分子式为C5H10,由于戊烯有2种,故三种烯烃为:CH2=CHCH(CH3)2,名称为3-甲基-1-丁烯,CH3CH=C(CH3)2,名称为2-甲基-2-丁烯,CH3CH2C(CH3)=CH2,名称为2-甲基-1-丁烯,
故答案为:3-甲基-1-丁烯;2-甲基-2-丁烯;2-甲基-1-丁烯.
点评 本题考查有机物分子式确定、同分异构体书写,难度中等,关键是计算确定分子式,注意根据中学常见烃解答.

练习册系列答案
相关题目
8.向含0.14molNa2CO3的溶液中逐滴加入含HCl 0.20mol的稀盐酸,待充分反应后,溶液中各溶质的物质的量正确的是( )
| 物质 n/mol 选项 | Na2CO3 | HCl | NaCl | NaHCO3 |
| A | 0 | 0 | 0.20 | 0.08 |
| B | 0.04 | 0 | 0.20 | 0 |
| C | 0 | 0.06 | 0.14 | 0.14 |
| D | 0 | 0 | 0.06 | 0.08 |
| A. | A | B. | B | C. | C | D. | D |
9.在盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后( )
| A. | 溶液的pH将增大 | B. | 钠离子数和碳酸根离子数的比变小 | ||
| C. | 溶液浓度增大并有晶体析出 | D. | 溶液浓度不变,有晶体析出 |
6.下列关于二氧化硅的说法中错误的是( )
| A. | 同二氧化碳一样,二氧化硅分子是由一个硅原子和两个氧原子构成的 | |
| B. | 通常状况下,二氧化碳为气态,二氧化硅为固体 | |
| C. | SiO2同CO2一样也能与CaO反应生成盐 | |
| D. | SiO2仅用来表示二氧化硅的组成,其基本结构单元为正四面体,不仅存在于二氧化硅晶体中,而且存在于所有硅酸盐矿石中 |
13.下列各组离子,能在溶液中大量共存的是( )
| A. | Ca2+、Al3+、NO3-、Cl- | B. | H+、Fe2+、SO42-、NO3- | ||
| C. | K+、NH4+、CO32-、OH-、 | D. | Na+、Mg2+、CO32-、Br- |
10.有机物A由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:(提示:请注意氢谱中峰的高度比)
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | (1)有机物A的相对分子质量为:90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使 其产物依次通过足量无水硫酸铜粉末、足量石灰水,发现硫酸铜粉末增重5.4g,石灰水中有30.0g白色沉淀生成. | (2)9.0g有机物A完全燃烧时,经计算: 生成CO2共为0.3mol, 生成的H2O0.3mol. 有机物A的分子式C3H6O3. |
| (3)经红外光谱测定,证实其中含有O-H键,-COOH基团,C-H键;经核磁共振氢谱的测定,其核磁共振氢谱图 如: 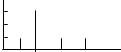 | (3)A的结构简式 . . |
| (4)如果经红外光谱测定,A的一种同分异构体中,存在O-H键, 还含有醛基,C-O键,  核磁共振氢谱的测定, 其核磁共振氢谱图如右: | (4)A的这种同分异构体的结构简式为: CH2(OH)CH(OH)CHO. |
| (5)如果经红外光谱测定,A的一种同分异构体中,存在O-H键,还含有C=O,C-O键, 核磁共振氢谱的测定, 其核磁共振氢谱图如: 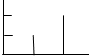 | (5)A的这种同分异构体的结构简式为: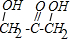 . . |
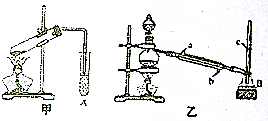 某化学兴趣小组用甲、乙两套装置(如图所示)进行甲酸(HCOOH)与甲醇(CH3OH)酯化反应的实验,回答以下问题:
某化学兴趣小组用甲、乙两套装置(如图所示)进行甲酸(HCOOH)与甲醇(CH3OH)酯化反应的实验,回答以下问题: