题目内容
【题目】(1)立方烷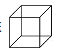 它的六氯代物有____种。
它的六氯代物有____种。
(2)  分子中最多有个____原子共面.
分子中最多有个____原子共面.
(3)① ![]() 的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
②聚合物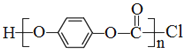 的单体是__________________。
的单体是__________________。
(4)①写出![]() 与足量溴水反应的化学方程式__________。
与足量溴水反应的化学方程式__________。
②写出 与足量NaOH溶液反应的化学方程式________。
与足量NaOH溶液反应的化学方程式________。
【答案】 3 23 2-甲基-1,3-丁二烯 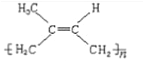
![]() 、
、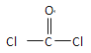
![]() +3Br2→
+3Br2→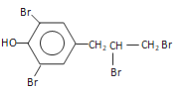 +2HBr
+2HBr 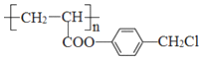 +3nNaOH→
+3nNaOH→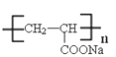 +n
+n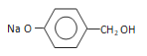 +nNaCl。
+nNaCl。
【解析】(1)考查同分异构体数目的判断,立方烷分子式为C8H8,六氯代物具有同分异构体的数目与二氯代物具有同分异构体的数目相同,两个氯原子在边长、面对角线、体角线,因此有三种符合题意的同分异构体;(2)考查共面,根据苯空间构型平面正六边形,甲烷空间构型为正四面体,以及三点确定平面,最多有23个原子共面;(3)考查有机物的命名、顺反结构、单体的判断,①按照烯烃的命名原则,此二烯烃的名称为2-甲基-1,3-丁二烯;此烯烃能发生加聚反应,顺式聚合物的结构简式为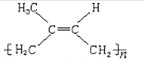 ;②形成此聚合物的反应类型为缩聚反应,其单体为
;②形成此聚合物的反应类型为缩聚反应,其单体为![]() 、
、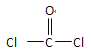 ;(4)考查有机物化学反应方程式的书写,①此有机物中含有碳碳双键,与溴水发生加成反应,含有酚羟基,能与溴水发生取代反应,其反应方程式为
;(4)考查有机物化学反应方程式的书写,①此有机物中含有碳碳双键,与溴水发生加成反应,含有酚羟基,能与溴水发生取代反应,其反应方程式为![]() +3Br2→
+3Br2→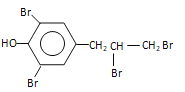 +2HBr;②含有酯基和氯原子,因此与足量NaOH溶液反应的方程式为:
+2HBr;②含有酯基和氯原子,因此与足量NaOH溶液反应的方程式为: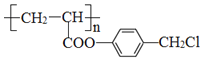 +3nNaOH→
+3nNaOH→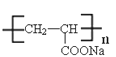 +n
+n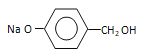 +nNaCl。
+nNaCl。

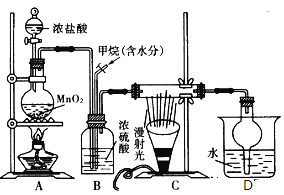
【题目】红帘石矿的主要成分为Fe3O4、Al2O3、MnCO3、Mg0少量MnO2等。工业上将红帘石处理后运用阴离子膜电解法的新技术提取金属钰并制得绿色高效的水处理剂(K2FeO4)。工业流程如下:
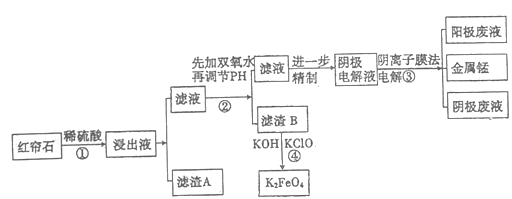
(1)在稀硫酸浸取矿石的过程中,MnO2可将Fe2+氧化为Fe3+,写出该反应的离子方程式:________。
(2)浸出液中的阳离子除H+、Fe2+、Fe3+外还有_______(填离子符号)。
(3)已知:不同金属离子生成生成氢氧化物沉淀所需的pH如下表:
离子 | Fe3+ | A13+ | Fe2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.6 |
完全沉淀的pH | 3.7 | 4.7 | 9.6 | 9.8 | 11.1 |
步骤②中调节溶液的pH等于6,调节pH的试剂最好选用下列哪种试剂:_______(填选项字母,下同)滤渣B除掉杂质后可进一步制取K2FeO4,除掉滤渣B中杂质最好选用下列哪种试剂:_____。
a.稀盐酸 b.KOH c.氨水 d.MnCO3 e.CaCO3
(4)滤渣B经反应④生成高效水处理剂的离子方程式_______________。
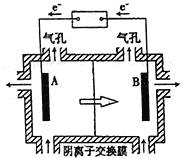
(5)电解装置如图所示,箭头表示溶液中阴离子移动的方向;则与A电极连接的是直流电源的_____极。阳极电解液是稀硫酸,若阴极上只有锰单质析出,当生成11g锰时,另一个电极上产生的气体在标准状况下的体积为________。