题目内容
【题目】在2L密闭容器中加入4molSO2和2molO2,发生下列反应2SO2(g)+O2(g)![]() 2SO3(g),
2SO3(g),
(1)若充分反应后能否得到4molSO3?为什么?__________________________
(2)若经5s后,剩下的SO2为2.5mol,则用O2表示的反应速率是多少?5s末SO3浓度是多少?
______________、__________
【答案】不能, 可逆反应不能完全进行 0.075 mol·L-1·S-1 0.75 mol·L-1
【解析】
(1)不能,该反应是可逆反应,加入4molSO2和2molO2不能完全转化为4molSO3。
(2)2SO2(g)+O2(g)![]() 2SO3(g),这里用浓度表示(mol/L)
2SO3(g),这里用浓度表示(mol/L)
起 2 1 0
转 0.75 0.375 0.75
平 1.25 0.625 0.75
v(O2)= ![]() =
=![]() mol·L-1·s-1= 0.075mol·L-1·s-1,易知5s末SO3浓度是0.75 mol·L-1。
mol·L-1·s-1= 0.075mol·L-1·s-1,易知5s末SO3浓度是0.75 mol·L-1。

【题目】为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
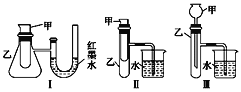
(1)上述3个装置中,不能证明“铜与浓硝 酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)___________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入 适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是______________,说明该反应属于_____ (填“吸热”或“放热”)反应。
(3)为定量测定(2)中反应的反应热,使50 mL 0.50 mol·L-1盐酸与50 mL0.55 mol·L-1NaOH溶液在简易量热计中进行中和反应.回答下列问题:
①该实验中NaOH的浓度大于HCl的浓度的作用是_________________________。
②实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
化学键 | C—H | C—F | H—F | F—F |
键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_______________。
【题目】下表列出了①~⑨九种元素在周期表中的位置:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑧ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑨ |
请按要求回答下列问题。
(1)元素④的名称是______,元素④在周期表中所处位置___________,从元素原子得失电子的角度看,元素④具有____________(填“氧化性”或“还原性”)。
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:_____________________(写氢化物的化学式)。
(3)元素⑦的原子结构示意图是____________。
(4)写出元素⑤形成的单质在氧气中燃烧的化学方程式________________,这一反应是___________(填“吸热”或“放热”)反应。
(5)用电子式表示①与⑨反应得到的化合物的形成过程_______________________。