题目内容
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,该反应达到平衡状态所需时间是_________。
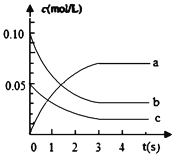
(2)上图中表示NO2的浓度变化曲线是_______________。
(3)用NO表示从0~2s内该反应的平均速率v=________。
(4)v(NO):v(O2) = ______________。
(5)达到平衡状态时O2的转化率为________。
【答案】 3s a 0.03mol/(L·s) 2:1 70%
【解析】试题(1)达到平衡状态时,体系中反应物、生成物浓度不再改变;
(2)反应中NO2的浓度增大;(3)根据![]() ,计算用NO表示从0~2s内该反应的平均速率;
,计算用NO表示从0~2s内该反应的平均速率;
(4)v(NO):v(O2)=系数比;
(5) O2的转化率=![]() 。
。
解析:(1)达到平衡状态时,体系中反应物、生成物浓度不再改变,3s后c(NO)不再变化,达到平衡状态所需时间是3s;
(2)反应中NO2的浓度增大,表示NO2的浓度变化曲线是a;
(3)根据![]() ,用NO表示从0~2s内该反应的平均速率v=
,用NO表示从0~2s内该反应的平均速率v=![]() 0.03mol/(L·s);
0.03mol/(L·s);
(4)v(NO):v(O2)= 2:1
(5) O2的转化率=![]() =
=![]() 70%。
70%。

【题目】葡萄酒常用Na2S2O5作抗氧化剂。中华人民共和国国家标准(G112760-2011)规定葡萄酒中抗氧化剂的残留量(以游离SO2计算)不能超过0.25g/L。某化学兴趣小组制备并对SO2的化学性质和用途进行探究,探究过程实验装置如下图,并收集某葡萄酒中SO2,对其含量进行测定。(夹持仪器省略)
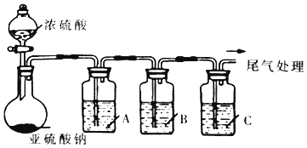
(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
试剂 | 作用 | |
A | _____________ | 验证SO2的还原性 |
B | Na2S溶液 | _____________ |
C | 品红溶液 | ______________ |
②A中发生反应的离子方程式为______________________________________
(2)该小组收集某300.00mL葡萄酒中SO2,然后用0.0900 mol/L NaOH标准溶液进行滴定,滴定前排气泡时,应选择下图中的_________(填序号);若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积_____(填序号)(①= 10mL;②=40mL; ③<10mL;④>40mL)

(3)该小组在实验室中先配制0.0900 mol/L NaOH标准溶液,然后再用其进行滴定。下列操作会导致测定结果偏高的是________。
A.未用NaOH标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.配制溶液定容时,俯视刻度线
E.中和滴定时,观察标准液体积读数时,滴定前仰视,滴定后俯视
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为_______g/L。