题目内容
【题目】现有浓度均为0.1 mol/L的下列溶液:
①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)___________________________。
(2)④、⑤、⑦、⑧四种溶液中NH4+浓度由大到小的顺序是(填序号)________ 。
(3)将②、③混合后,若溶液呈中性,则消耗两溶液的体积为 ② ________ ③(填“>”、“<”或“=”)溶液中的离子浓度由大到小的顺序为______________________________
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液,判断:
①其中有两种粒子的物质的量之和一定等于0.010 mol,它们是________和________。
②溶液中c(CH3COO-)+n(OH-)-n(H+)=________ mol。
【答案】④②③①⑦④⑤⑧>c(Na+) =c(CH3COO-) >c(H+) =c( OH-)CH3COOHCH3COO-0.006
【解析】
(1)水在溶液中存在电离平衡H2O![]() H++OH- ,所以酸或碱均是抑制水的电离,如果氢离子浓度和OH― 如果相同,对水的电离抑制程度就相同的。盐的水解可以促进水的电离。硫酸是二元强酸,醋酸是一元弱酸,氢氧化钠是一元强碱,氯化铵溶于水存在水解平衡,所以由水电离出的H+ 浓度由大到小的顺序是④②③①;(2)氨水是弱碱部分电离,所以NH4+浓度最小。另外三种属于铵盐,NH4+ 水解显酸性,⑦中能电离出大量的氢离子,抑制其水解,⑤中阳离子和阴离子均水解,相互促进。所以溶液中NH4+浓度由大到小的顺序是⑦④⑤⑧;(3)②和③等体积混合后,二者恰好反应生成醋酸钠,醋酸钠水解显碱性,所以混合液中各离子浓度由大到小的顺序是c(Na + )> c(CH3COO- ) >c(OH-)>c(H+);(4)根据物料守恒可知,0.010mol CH3COONa在溶液中以CH3COOH和CH3COO-存在,n(CH3COOH)+n(CH3COO-)=0.010mol,故答案为:CH3COOH;CH3COO-;(2)溶液遵循电荷守恒,存在:n(H+)+n(Na+)=n(Cl-)+n(CH3COO-)+n(OH-),则n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol。
H++OH- ,所以酸或碱均是抑制水的电离,如果氢离子浓度和OH― 如果相同,对水的电离抑制程度就相同的。盐的水解可以促进水的电离。硫酸是二元强酸,醋酸是一元弱酸,氢氧化钠是一元强碱,氯化铵溶于水存在水解平衡,所以由水电离出的H+ 浓度由大到小的顺序是④②③①;(2)氨水是弱碱部分电离,所以NH4+浓度最小。另外三种属于铵盐,NH4+ 水解显酸性,⑦中能电离出大量的氢离子,抑制其水解,⑤中阳离子和阴离子均水解,相互促进。所以溶液中NH4+浓度由大到小的顺序是⑦④⑤⑧;(3)②和③等体积混合后,二者恰好反应生成醋酸钠,醋酸钠水解显碱性,所以混合液中各离子浓度由大到小的顺序是c(Na + )> c(CH3COO- ) >c(OH-)>c(H+);(4)根据物料守恒可知,0.010mol CH3COONa在溶液中以CH3COOH和CH3COO-存在,n(CH3COOH)+n(CH3COO-)=0.010mol,故答案为:CH3COOH;CH3COO-;(2)溶液遵循电荷守恒,存在:n(H+)+n(Na+)=n(Cl-)+n(CH3COO-)+n(OH-),则n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol。

 一课一练课时达标系列答案
一课一练课时达标系列答案【题目】(1)汽车尾气中的主要污染物是NO、NO2和CO。用NaOH溶液可吸收NO、NO2,当n(NO)﹕n(NO2)=1时只生成一种盐,这种盐的化学式为__________。
(2)金属铬(Cr)的英文是Chromium,原意是颜色,因为它的化合物都有美丽的颜色。如表是几种常见铬的化合物或离子的水溶液的颜色:
离子或化合物 | Cr2O72- | Cr(OH)3 | Cr3+ | CrO2- | CrO42- |
颜色 | 橙色 | 灰蓝色 | 蓝紫色 | 绿色 | 黄色 |
含铬元素的化合物可以发生如图一系列变化:
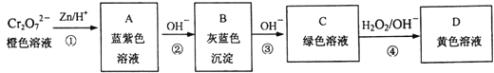
①写出反应④的离子方程式:______________________________________。
②结合上述转化图及所学知识,请分析向NaCrO2溶液中逐滴加入过量稀硫酸的现象为______。
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,该反应达到平衡状态所需时间是_________。
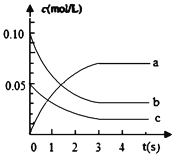
(2)上图中表示NO2的浓度变化曲线是_______________。
(3)用NO表示从0~2s内该反应的平均速率v=________。
(4)v(NO):v(O2) = ______________。
(5)达到平衡状态时O2的转化率为________。