题目内容
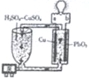
【题目】四种短周期主族元素在周期表中的位置如图,则下列说法错误的是( )
![]()
A.若X单质即可与强酸,也可与强碱溶液反应,则M单质可做半导体
B.若M、Z、Y皆存在简单阴离子,则离子半径:M>Z>Y
C.若Y的氢化物的水溶液呈碱性,则X的氧化物不与任何酸反应
D.若四种元素的原子序数之和为56,则Z的单质可以用作自来水的消毒剂
【答案】C
【解析】
由四种短周期主族元素在周期表中的位置可知,Y为第二周期元素,X、M、Z为第三周期元素,且Y、M同主族。
A. 若X单质即可与强酸,也可与强碱溶液反应,则X是铝,M单质是硅,可做半导体,故A正确;
B. 电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小,则简单阴离子半径M>Z>Y,故B正确;
C. Y的氢化物水溶液呈碱性,Y为N,X为Si,二氧化硅与HF酸反应,故C错误;
D. 若四种元素的原子序数之和为56,令M的为x,x-1+x+x+1+x-8=56,x=16,M为S,Z为Cl,则Z的单质可以用作自来水的消毒剂,故D正确;
故选C。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) = CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) = 2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) = 2NO(g) △H 3 =+180.5 kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_______。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(104mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(103mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L1·s1。
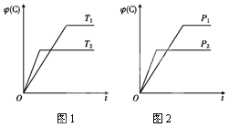
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是___________。判断L1、L2的大小关系,并简述理由:_________。

(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_________(填“>”、“<”或 “=”)k逆增大的倍数。
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =_____________。(保留一位小数)