题目内容
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气![]() 进行此实验,所用仪器如图:
进行此实验,所用仪器如图:
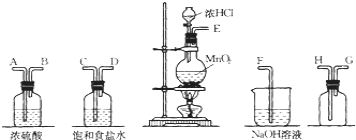
![]() 连接上述仪器的正确顺序是:____________。
连接上述仪器的正确顺序是:____________。
![]() 气体发生装置中进行的反应化学方程式是 ______ ;当
气体发生装置中进行的反应化学方程式是 ______ ;当![]() 参与反应时,被氧化的HCl的质量为 ______ 。
参与反应时,被氧化的HCl的质量为 ______ 。
![]() 在装置中:
在装置中:![]() 饱和食盐水的作用是 ______。
饱和食盐水的作用是 ______。
![]() 化学实验中检验是否有
化学实验中检验是否有![]() 产生常用湿润的淀粉
产生常用湿润的淀粉![]() 试纸
试纸![]() 如果有
如果有![]() 产生,可观察到的现象是 ______ ,写出反应方程式 ______ 。
产生,可观察到的现象是 ______ ,写出反应方程式 ______ 。
![]() 写出尾气吸收装置中进行的反应的化学方程式 ______ 。
写出尾气吸收装置中进行的反应的化学方程式 ______ 。
【答案】ECDABHGF MnO2+4HC1(浓)![]() MnCl2+Cl2↑+2H2O 36.5g 除去氯气中的氯化氢 试纸变蓝 Cl2+2KI=KCl+I2 Cl2+2NaOH=NaCl+NaClO+H2O
MnCl2+Cl2↑+2H2O 36.5g 除去氯气中的氯化氢 试纸变蓝 Cl2+2KI=KCl+I2 Cl2+2NaOH=NaCl+NaClO+H2O
【解析】
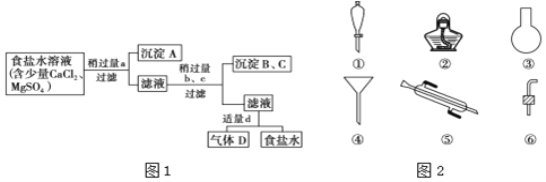
二氧化锰和浓盐酸反应生成氯气,含有氯化氢和水蒸气,先用饱和食盐水除去氯化氢,然后用浓硫酸除去水蒸气,然后用向上排气法收集氯气,最后用氢氧化钠做尾气处理。据此解答。
(1)二氧化锰和浓盐酸反应生成氯气,含有氯化氢和水蒸气,先用饱和食盐水除去氯化氢,然后用浓硫酸除去水蒸气,然后用向上排气法收集氯气,最后用氢氧化钠做尾气处理,所以连接顺序为:ECDABHGF;
(2)反应方程式为:MnO2+4HC1(浓)![]() MnCl2+Cl2↑+2H2O;当
MnCl2+Cl2↑+2H2O;当![]() 参与反应时,被氧化的氯化氢为1mol,质量为36.5g;
参与反应时,被氧化的氯化氢为1mol,质量为36.5g;
(3)饱和食盐水的作用是除去氯气中的氯化氢;
(4)氯气和碘化钾反应生成碘和氯化钾,碘遇淀粉变蓝,所以现象为试纸变蓝,方程式为:Cl2+2KI=KCl+I2;
(5)氯气和氢氧化钠反应生成氯化钠和次氯酸钠和水,方程式为:Cl2+2NaOH=NaCl+NaClO+H2O

 阅读快车系列答案
阅读快车系列答案【题目】制备金属钾的反应:Na+KCl ![]() K+NaCl,有关沸点的数据如下:
K+NaCl,有关沸点的数据如下:
物质 | K | Na | KCl | NaCl |
沸点(°C) | 759 | 883 | 1420 | 1465 |
下列说法不正确的是
A.该反应说明,Na的金属性强于K
B.850°C时,钾蒸气逸出,平衡正向移动,KCl转化率增大
C.升温至900°C,收集金属钾,钾的纯度会降低
D.金属钾中含有杂质钠,可通过真空蒸馏的方法分离提纯
【题目】工业合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g),对其研究如下:
2NH3(g),对其研究如下:
(1)已知H—H键能为436kJ·mol-1,N—H键能为391kJ·mol-1,N≡N键的键能是946kJ·mol-1,则上述反应的ΔH=_________________。
(2)上述反应的平衡常数K的表达式为____________,若反应方程式改写为NH3(g)![]() N2(g)+
N2(g)+![]() H2(g),则平衡常数K1=____________________(用K表示)。
H2(g),则平衡常数K1=____________________(用K表示)。
(3)在773K时,分别将2mol N2和6mol H2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3)/mol | 0 | 1.00 | m | 1.80 | 1.98 | 2.00 | 2.00 |
①表格中m=_______________/span>,15~25min内,v(N2)=_______________。
②该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度均为3mol·L-1,此时v正_______v逆(填“>”、“<”或“=”)。
③由表中的实验数据计算得到“浓度~时间”的关系可用图中的曲线表示,表示c(N2)~t的曲线是______________(填“甲”、“乙”或“丙”)。在此温度下,若起始充入4mol N2和12mol H2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为_________________。

(4)Marnellos和Stoukides采用电解法合成氨,实现了常压合成和氮气的高转化率。该方法用SCY陶瓷将两极隔开,SCY陶瓷具有高质子导电性,其作用是传导H+,则阴极的电极反应为____________________。