题目内容
9.同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )| A. | 它是一种共价化合物 | B. | 它不可能与NaOH溶液反应 | ||
| C. | 它既含离子键又含共价键 | D. | 它受热时不会分解 |
分析 同族元素所形成的同一类型的化合物,其结构和性质往往相似,则化合物PH4I的结构和性质与NH4Cl相似,根据氯化铵的结构、性质分析解答.
解答 解:化合物PH4I的结构和性质与NH4Cl相似,
A.氯化铵是离子化合物,则PH4I也是离子化合物,故A错误;
B.氯化铵和碱能反应,所以PH4I也能和碱反应,故B错误;
C.氯化铵中含有离子键、共价键,则PH4I中也含离子键和共价键,故C正确;
D.氯化铵受热分解为氨气和HCl,则该化合物受热也可以分解为PH3和HI,故D错误;
故选C.
点评 本题考查了物质结构、性质的判断,利用知识迁移的方法分析该化合物性质,同时考查学生获取信息并灵活运用信息的能力,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.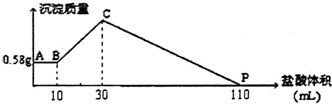 把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浑浊液中,逐渐加入1mol/L盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示.则混合物中NaOH质量为( )
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浑浊液中,逐渐加入1mol/L盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示.则混合物中NaOH质量为( )
 把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浑浊液中,逐渐加入1mol/L盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示.则混合物中NaOH质量为( )
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浑浊液中,逐渐加入1mol/L盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示.则混合物中NaOH质量为( )| A. | 3.6g | B. | 4g | C. | 4.4g | D. | 4.8g |
20.下列有关氮气的叙述不正确的是( )
| A. | 氮分子为非极性分子 | |
| B. | 在灯泡中充入氮气可防止钨丝被氧化 | |
| C. | 氮元素比磷元素非金属性强,所以硝酸比磷酸酸性强 | |
| D. | 氮分子中有2个σ键1个π键 |
17.已知A、B、C、D的原子序数都不超过18,它们的离子aA2+、bB+、cC2-、dD-均具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A2+>B+>C2->D- | |
| C. | 单质还原性:B>A,单质氧化性:D>C | |
| D. | 离子还原性:C2->D-,离子氧化性:B+>A2+ |
4.下列有机物中,不能与金属钠反应放出氢气的是( )
| A. | 乙醇 | B. | 乙烯 | C. | 乙酸 | D. | 碳酸钠溶液 |
14.下列微粒中半径最小的( )
| A. | Na+ | B. | Al3+ | C. | K+ | D. | S2- |
1.下列关于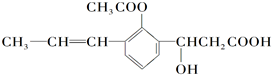 的叙述,错误的是( )
的叙述,错误的是( )
 的叙述,错误的是( )
的叙述,错误的是( )| A. | 可以和溴水反应 | |
| B. | 该物质中含有羟基、羧基、碳碳双键和醚键 | |
| C. | 可以发生消去和取代反应 | |
| D. | 1 mol该最多可以和4 mol H2发生加成反应 |
19.生活中处处有化学,下列表述不正确的是( )
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 苯酚有毒,但可用于杀菌消毒 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 食醋的主要成分是醋酸,它是一种弱酸 |
