题目内容
1.下列关于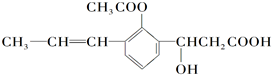 的叙述,错误的是( )
的叙述,错误的是( )| A. | 可以和溴水反应 | |
| B. | 该物质中含有羟基、羧基、碳碳双键和醚键 | |
| C. | 可以发生消去和取代反应 | |
| D. | 1 mol该最多可以和4 mol H2发生加成反应 |
分析 由结构可知,分子中含碳碳双键、-COOC-、-OH、-COOH,结合烯烃、酯、醇、羧酸的性质来解答.
解答 解:A.含碳碳双键,可与溴水发生加成反应,故A正确;
B.该物质中含有羟基、羧基、碳碳双键,不含醚键,故B错误;
C.含-OH可发生消去、取代反应,故C正确;
D.苯环、双键与氢气发生加成反应,则1 mol该最多可以和4 mol H2发生加成反应,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、醇性质的考查,题目难度不大.

练习册系列答案
相关题目
12.下列物质不能由单质直接化合生成的是( )
| A. | CuCl2 | B. | NO2 | C. | FeCl3 | D. | Na2O2 |
9.同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )
| A. | 它是一种共价化合物 | B. | 它不可能与NaOH溶液反应 | ||
| C. | 它既含离子键又含共价键 | D. | 它受热时不会分解 |
6.下列关于元素的叙述正确的是( )
| A. | 金属元素与非金属元素能形成共价化合物 | |
| B. | Cl-、S2-、Ca2+、K+半径逐渐减小 | |
| C. | 目前使用的元素周期表中,最长的周期含有36种元素 | |
| D. | 多电子原子中,在离核较近的区域内运动的电子能量较高 |
13.下列各项中表达正确的是( )
| A. | 第三周期元素形成的最高价氧化物对应的水化物中,酸性最强的是HClO4 | |
| B. | 水分子很稳定性是因为水分子间易形成氢键 | |
| C. | 用电子式表示HCl形成过程:H-+${\;}_{\;}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$→H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| D. | 第VⅡA族元素形成的氢化物中沸点最高的是HI |
10.温度为500℃时,反应4NH3+5O2=4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为( )
| A. | v(O2)=0.01mol/(L•s) | B. | v(NO)=0.08mol/(L•s) | ||
| C. | v(H2O)=0.002mol/(L•s) | D. | v(NH3)=0.002mol/(L•s) |
11.下列叙述正确的是( )
| A. | 同周期元素的原子半径以ⅦA族的为最大 | |
| B. | 在周期表中0族元素的电负性最大 | |
| C. | ⅠA族元素的原子,其半径越大第一电离能越小 | |
| D. | 所有主族元素的原子形成单原子离子时的最高价数都和它的族数相等 |
