题目内容
7.NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1 mol CO2中含有原子数NA | |
| B. | 1mol/L的硫酸钠溶液中,所含Na+数为2NA | |
| C. | 标准状况下,11.2 L水所含分子数为0.5 NA | |
| D. | 1 mol Fe和足量盐酸完全反应失去的电子数为2NA |
分析 A、CO2中含3个原子;
B、溶液体积不明确;
C、标况下,水为液态;
D、铁与盐酸反应变为+2价.
解答 解:A、CO2中含3个原子,故1mol二氧化碳中含3mol原子即3NA个,故A错误;
B、溶液体积不明确,故溶液中钠离子的个数无法计算,故B错误;
C、标况下,水为液态,不能根据气体摩尔体积来计算其物质的量,故C错误;
D、铁与盐酸反应变为+2价,故1mol铁失去2mol即2NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
18.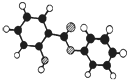 萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )
萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )
 萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )
萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )| A. | 萨罗的分子式为C13H10O3 | |
| B. | 1mol萨罗与浓溴水反应,需要消耗3mol Br2 | |
| C. | 1mol萨罗发生水解,需要消耗3mol NaOH | |
| D. | 萨罗经水解、分离、提纯可得到纯净的苯酚和水杨酸(邻羟基苯甲酸) |
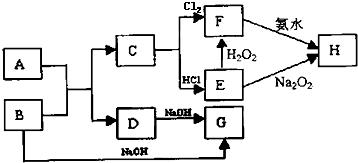
15.某同学在探究废干电池内的黑色固体回收利用时,进行如下所示实验:

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2和石墨粉等物质.请回答以下问题:
(1)操作②玻璃棒的作用是引流;操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、坩埚 和三脚架;
(2)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(填化学式).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2(填化学式).
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2和石墨粉等物质.请回答以下问题:
(1)操作②玻璃棒的作用是引流;操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、坩埚 和三脚架;
(2)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(填化学式).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2(填化学式).
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 有白色沉淀产生 | 含有Cl- |
| 2检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ |
17.下列说法正确的是( )
| A. | 乙醇易溶于水,难溶于有机溶剂 | |
| B. | 苯的分子结构中含有碳碳双键 | |
| C. | 乙烯通入酸性KMn04溶液中,紫色褪去 | |
| D. | 苯的硝化、乙烯使高锰酸钾酸性溶液褪色的反应都属于取代反应 |
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示: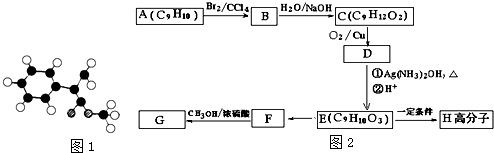
 ;
;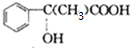 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$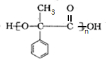 +(n-1)H2O.
+(n-1)H2O.