题目内容
下图各装置中,不能构成原电池的是(烧杯中所盛液体都是稀硫酸)( )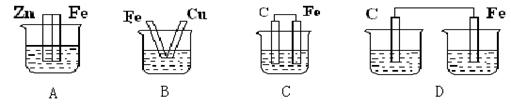
D
解析试题分析:原电池的构成条件是:①两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,A、B和C都符合原电池的构成条件,所以能形成原电池,D中不能构成闭合回路,所以不能构成原电池,选D。
考点:考查原电池的构成条件。

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
某小组为研究电化学原理,设计如图装置。下列叙述错误的是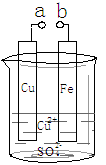
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动 |
| D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色 |
将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是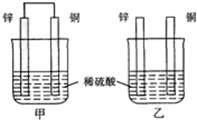
| A.两烧杯中溶液的pH均增大 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中铜片表面均无气泡产生 |
| D.甲、乙溶液均变蓝色 |
某金属元素R的硝酸盐R(NO3)n溶液用Pt电极电解,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的原子量为M,下列叙述中不正确的是 ( )
A.电路中通过电子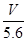 mol mol | B.n=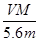 |
C.溶液中H+增加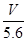 mol mol | D.n=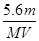 |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )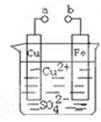
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
一种充电电池放电时的电极反应为H2+2OH—2e-=2H2O;NiO(OH)+H2O+e-=Ni(OH)2+OH-,当为电池充电时,与外电源正极连接的电极上发生的反应是
| A.H2O的还原 | B.NiO(OH)的还原 | C.H2的氧化 | D.NiO(OH) 2的氧化 |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大。)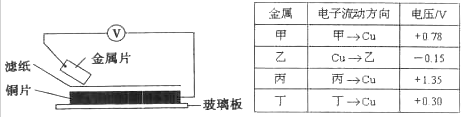
依据记录数据判断,下列结论中正确的是
| A.将甲、乙形成的合金露置在空气中,甲先被腐蚀 |
| B.金属乙能从硫酸铜溶液中置换出铜 |
| C.在四种金属中丙的还原性最弱 |
| D.甲、丁若形成原电池时,甲为正极 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2═4Fe(OH)3 |
| B.2Fe+2H2O+O2═2Fe(OH)2 |
| C.2H2O+O2+4e-═4OH- |
| D.Fe-3e-═Fe3+ |
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。以Al—H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极)。下列说法不正确的是 
| A.燃料电池的总反应为:2Al+3HO2-= 2AlO2- + OH- +H2O |
| B.电极b是正极,且反应后该电极区pH增大 |
| C.电解过程中,电子的流向由a→b→c→d. |
| D.电解时,Al消耗2.7g,则产生氮气标准状况下为1.12L |