题目内容
【题目】N2H4(联氨又称肼)一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________________。
(2)N2H4是火箭升空需要高能的燃料,工业上利用N2和H2可以合成联氨(N2H4)等。已知:
N2(g)+2O2(g)= N2O4 (l) △H=-19.5kJ·mol-1
2H2(g)+O2(g) =2H2O(g) △H =-483.6 kJ·mol-1
2N2H4(1) +N2O4(l)= 3N2(g)+4H2O(g) △H = -1048.9 kJ·mol-1
写出N2和H2合成液态联氨(N2H4)的热化学方程式______________________________。火箭升空经常用联氨和N2O4反应作为火箭推进剂,其主要原因为______________________________。
(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH--4e-═O2↑+2H2O,则阴极的电极反应式为___________________。有人提出,可以设计反应2CO= 2C+O2(△H >0)来消除CO的污染。请判断上述反应是否能自发进行并说明理由_____________________________。
【答案】 NaClO+2NH3=N2H4+NaCl+H2O N2(g)+2H2(g)=N2H4(l) ΔH= +50.6 kJ·mol1 放出大量热,产生大量气体 CO2+2e-+H2O=CO+2OH-或 2CO2+4e-+2H2O=2CO+4OH- 不能 ,因该反应的ΔH>0 , ΔS<0,所以反应不能自发进行
【解析】(1)氨气被次氯酸钠溶液氧化生成肼,次氯酸钠被还原生成氯化钠,结合原子守恒配平书写反应的化学方程式为:2NH3+NaClO═N2H4+NaCl+H2O,故答案为:2NH3+NaClO═ N2H4+NaCl+H2O;
(2)①N2(g)+2O2(g)= N2O4 (l) △H=-19.5kJ·mol-1,②2H2(g)+O2(g) =2H2O(g) △H =-483.6 kJ·mol-1,③2N2H4(1) +N2O4(l)= 3N2(g)+4H2O(g)△H = -1048.9 kJ·mol-1,依据热化学方程式和盖斯定律计算,将②-①×![]() -③×
-③×![]() 得:N2(g)+2H2(g)=N2H4(l) ΔH=(-483.6 kJ·mol-1)-(-19.5kJ·mol-1)×
得:N2(g)+2H2(g)=N2H4(l) ΔH=(-483.6 kJ·mol-1)-(-19.5kJ·mol-1)×![]() -(-1048.9 kJ·mol-1)×
-(-1048.9 kJ·mol-1)×![]() = +50.6 kJ·mol1,根据反应③可知,联氨和N2O4反应放出大量热且产生大量气体,因此可作为火箭推进剂,故答案为:N2(g)+2H2(g)=N2H4(l) ΔH= +50.6 kJ·mol1;反应放热量大,产生大量气体;
= +50.6 kJ·mol1,根据反应③可知,联氨和N2O4反应放出大量热且产生大量气体,因此可作为火箭推进剂,故答案为:N2(g)+2H2(g)=N2H4(l) ΔH= +50.6 kJ·mol1;反应放热量大,产生大量气体;
(3)2CO2═2CO+O2,CO可用作燃料,已知该装置的阳极反应为:4OH--4e-═O2↑+2H2O,阴极反应依据电子守恒总反应减去阳极反应得到:2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O ═ CO+2OH-);2CO═2C+O2 △H>0,△S<0,△H-T△S>0,反应一定不能自发进行,故答案为:2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O═CO+2OH-);不能,因该反应的ΔH>0,ΔS<0,所以反应不能自发进行。

【题目】I.SO2是一种重要的化工原料,其合理利用以及废气处理一直是化工研究的热点。
(1)氧元素在元素周期表中位于第______周期______族,硫原子核外有_____种能量不同的电子。
(2)元素的非金属性S比O______(填“强”或“弱”),从原子结构的角度解释原因:__________。
II.工业上利用反应SO2 + MnO2 → MnSO4 可以制备高纯 MnSO4,实验装置如下图:

(3)请标出反应SO2 + MnO2 → MnSO4的电子转移方向和数目____________
(4)在通入干燥空气的条件下,一段时间后,测得反应后溶液中的 n(SO42-)明显大于 n(Mn2+),请说明原因: ___________________。用化学方程式表示石灰乳的作用: ___________________。
III.SO2可用于处理含 Cr2O72-(铬元素化合价为+6)的废水,最后转化为铬沉淀(铬元素化合价为+3)除去。一种处理流程如下:
![]()
(5)NaHSO3与 Cr2O72-反应时,物质的量之比为__________。
【答案】 二 ⅥA 5 弱 硫原子半径大于氧原子半径,硫原子和氧原子的最外层电子数相等,硫原子的得电子能力比氧原子弱  在溶液中,空气中的氧气将二氧化硫氧化为 H2SO4 SO2+ Ca(OH)2→CaSO3+ H2O(或2SO2+2Ca(OH)2+O2→ 2CaSO4 + 2H2O) 3∶1
在溶液中,空气中的氧气将二氧化硫氧化为 H2SO4 SO2+ Ca(OH)2→CaSO3+ H2O(或2SO2+2Ca(OH)2+O2→ 2CaSO4 + 2H2O) 3∶1
【解析】试题分析:(1)氧原子核外有2个电子层,最外层有6个电子,硫原子核外电子排布式是1S22S22P63S23P4;(2)同主族元素最外层电子数相同,原子半径自上而下逐渐增大,得电子能力逐渐减弱,失电子能力逐渐增强;(3)反应SO2 + MnO2 → MnSO4中,硫元素化合价由+4升高为+6,锰元素化合价由+4降低为+2;(4)氧气能把二氧化硫氧化为 H2SO4;二氧化硫污染空气,用氢氧化钙能吸收二氧化硫;(5)NaHSO3与 Cr2O72-反应时,硫元素化合价由+4升高为+6,铬元素化合价由+6降低为+3,根据化合价升降相同计算物质的量之比。
解析:(1)氧原子核外有2个电子层,最外层有6个电子,所以氧元素在元素周期表中位于第二周期ⅥA族,硫原子核外电子排布式是1S22S22P63S23P4,有5个能级,所以有5种能量不同的电子;(2) 同主族元素最外层电子数相同,原子半径自上而下逐渐增大,得电子能力逐渐减弱,失电子能力逐渐增强,所以S非金属性比O弱;(3)反应SO2 + MnO2 → MnSO4中,硫元素化合价由+4升高为+6,硫失去2个电子,锰元素化合价由+4降低为+2,锰元素得到2个电子,所以电子转移方向和数目是 ;(4)氧气能把二氧化硫氧化为 H2SO4,所以反应后溶液中的 n(SO42-)明显大于 n(Mn2+);二氧化硫污染空气,氢氧化钙能吸收二氧化硫,反应方程式为SO2+ Ca(OH)2→CaSO3+ H2O;(5)NaHSO3与 Cr2O72-反应时,硫元素化合价由+4升高为+6,铬元素化合价由+6降低为+3,设NaHSO3与 Cr2O72-反应时的物质的量比为x∶y,根据化合价升降相同,2x=y×2×3,所以x∶y= 3∶1。
;(4)氧气能把二氧化硫氧化为 H2SO4,所以反应后溶液中的 n(SO42-)明显大于 n(Mn2+);二氧化硫污染空气,氢氧化钙能吸收二氧化硫,反应方程式为SO2+ Ca(OH)2→CaSO3+ H2O;(5)NaHSO3与 Cr2O72-反应时,硫元素化合价由+4升高为+6,铬元素化合价由+6降低为+3,设NaHSO3与 Cr2O72-反应时的物质的量比为x∶y,根据化合价升降相同,2x=y×2×3,所以x∶y= 3∶1。
点睛:氧化还原反应中,氧化剂得电子化合价降低,还原剂失电子化合价升高,根据氧化还原反应的升降规律,氧化剂得电子数一定等于还原剂失电子数。
【题型】综合题
【结束】
22
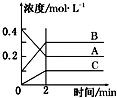
【题目】I.工业上可由氢气、氮气合成氨气,溶于水形成氨水。盐酸和氨水是实验室常见的电解质溶液。一定温度下,向2L 密闭容器中加入N2(g)和H2(g),发生反应:N2(g)+3H2(g)![]() 2NH3(g)+ Q(Q>0), NH3物质的量随时间的变化如右图所示。
2NH3(g)+ Q(Q>0), NH3物质的量随时间的变化如右图所示。

(1)0~2 min 内的平均反应速率 v(H2)=___________。
(2)该温度下,反应 N2(g)+3H2(g)![]() 2NH3(g)+ Q(Q>0)的平衡常数表达式K=______。其平衡常数K与温度T的关系如下表:
2NH3(g)+ Q(Q>0)的平衡常数表达式K=______。其平衡常数K与温度T的关系如下表:
T/ ℃ | 25 | 125 | 225 |
平衡常数 K | 4×106 | K1 | K2 |
试判断K1________K2(填写“>”“=”或“<”)。
(3)下列能说明合成氨反应已达到平衡状态的是______(填字母)(反应是在固定体积的密闭容器中进行的)
a.3v(N2) = v(H2)
b.容器内压强保持不变
c.混合气体的密度保持不变
d.25℃时,测得容器中c(NH3)=0.2 mol·L-1, c(H2) =c(N2) =0.01 mol·L-1
II.常温下,某同学将盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH 如下表。
实验编号 | 氨水浓度/mol·L-1 | 盐酸浓度/mol·L-1 | 混合溶液 pH |
① | 0. 2 | 0.2 | pH=x |
② | c | 0.2 | pH=7 |
请回答:
(4)①中所得混合溶液, pH_______7(填“>”“<”或“=”)。
②中 c___0.2(填“>”“<”或“=”),所得混合溶液中各离子浓度大小关系为_____________。
(5)请你再设计一个能证明一水合氨是弱电解质的方案。_____________。