题目内容
16.亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上.某学习小组针对亚硝酸钠设计了如下实验:实验Ⅰ制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3
设计制备装置如下(夹持装置略去):
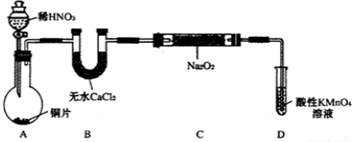
(1)如果没有B装置,C中发生的副反应有2Na2O2+2H2O=4NaOH+O2↑,2NO+O2=2NO2.
(2)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O.
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质.于是在A与B装置间增加了在A、B之间增加装有水的洗气瓶装置,改进后提高了NaNO2的纯度.
实验Ⅱ测定制取的样品中NaNO2的含量
步骤:a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10mL并振荡,制成标准色阶:
b.称量0.10g制得的样品溶于水配成500mL溶液.再取5mL待测液,加入1mL M溶液,后加蒸馏水至10mL振荡,与标准色阶比较.
| 试管编号 | ① | ② | ③ | ④ | ⑤ |
| NaNO2含量/mg•L-1 | 0 | 20 | 40 | 60 | 80 |
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量.设计并完成下列实验报告.
| 实验方案 | 实验现象 | 实验结论 |
| 取5mL 待测液,加入一定量的维生素C,振荡, 再加入1mL M溶液,加入至蒸馏水10mL,再振荡, 与④号色阶对比. | 紫红色比④色阶浅 | 维生素C 可以有效降低NaNO2的含量. |
分析 (1)金属铜和稀硝酸制得的一氧化氮中含有水,会和过氧化钠发生反应产生氧气,氧气极易把一氧化氮氧化;
(2)高锰酸钾具有氧化性,能将一氧化氮氧化,根据电子守恒配平方程式即可;
(3)硝酸具有挥发性,会干扰实验结果,据此回答分析;
(4)根据物质纯度计算公式纯度=$\frac{物质含量}{样品质量}$×100%;
(5)根据维生素C的作用以及要和(4)中的甲同学的实验方案形成对比试验,进行实验设计.
解答 解:(1)金属铜和稀硝酸制得的一氧化氮中含有水,水会和过氧化钠发生反应产生氧气,2Na2O2+2H2O=4NaOH+O2↑,生成的氧气极易把一氧化氮氧化为二氧化氮,即2NO+O2=NO2,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;2NO+O2=2NO2;
(2)高锰酸钾具有氧化性,能将一氧化氮氧化,反应的实质是:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O,
故答案为:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O;
(3)由于获得一氧化氮所用的硝酸具有挥发性,这样会干扰实验结果,可以在A、B之间增加装有水的洗气瓶,减小实验误差,
故答案为:在A、B之间增加装有水的洗气瓶;
(4)甲待测液颜色与④号色阶相同,则甲同学制得的样品中NaN02的纯度是$\frac{60×10{\;}^{-3}g×100}{0.1g}$×100%=60%,
故答案为:60%;
(5)要和(4)中的甲同学的实验方案形成对比试验,同样可以是先取5mL待测液,然后加入维生素C,并加入1 mLM溶液,最后加入蒸馏水至10mL,若紫红色比③色阶浅,说明亚硝酸钠的含量低,则可以证明维生素C可以有效降低NaNO2的含量.
故答案为:维生素C;加入至蒸馏水10mL;紫红色比④色阶浅.
点评 本题是一道实验方案的设计和探究题,考查学生分析和解决问题的能力,综合性强,难度大.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案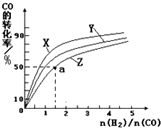 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式
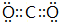 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等. 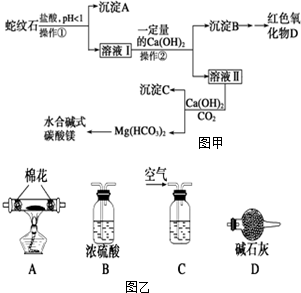 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)实验室完成操作①所用到的玻璃仪器有玻璃棒、漏斗、烧杯.
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为OH-+Al(OH)3═AlO2-+2H2O,再进行过滤、洗涤、加热(依次填写实验操作名称).
(4)操作②中应控制溶液pH的合理范围是C(填序号).
A.小于1.5 B.1.5~3.3 C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样7.28g于装置A的玻璃管中,请按由左-→右顺序将如图乙装置连接好(填序号,装置可重复使用)C-→B-→A-→B-→D-→B(或D),装置C应盛的试剂是氢氧化钠溶液.充分反应后,如果实验测得硬质玻璃管中剩余固体3.2g,共放出2.64g CO2气体,则x:y:z=3:1:3.
| A. | CH4→CO2 | B. | KMnO4→K2MnO4 | C. | SO2→SO32- | D. | H2O2→O2 |
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| D. | 氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |
| A. | 实验室可通过蒸馏的方法除去自来水中含有的氯离子等杂质制蒸馏水 | |
| B. | 将氢氧化钠稀溶液逐滴滴入氯化铁饱和溶液中,边滴边搅拌,可获得氢氧化铁胶体 | |
| C. | 由于氢氧化铁胶体带正电,所以电泳时阴极颜色加深 | |
| D. | 浓硫酸不慎溅到皮肤上,应该立即用大量水冲洗,然后涂上稀NaOH溶液 |

 如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).
如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).