题目内容
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
A.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=
 mol/L
mol/LB.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
A
解析试题分析:A、根据题给数据①知,0.1mol/L HA溶液和0.1mol/LKOH溶液等体积混合,恰好反应生成KA盐溶液,根据电荷守恒式知,c(OH-)=c(K+)+c(H+)-c(A-)= mol/L,错误;B、根据题给数据①知,0.1mol/L HA溶液和0.1mol/LKOH溶液等体积混合,恰好反应生成KA盐溶液,溶液PH常温下为9,说明溶液呈碱性,溶液中离子浓度大小为c(K+)>c(A-)>c(OH-)>c(H+),正确;C、根据题给数据②知,常温下混合后溶液PH=7,呈中性,则HA过量,溶液是HA和KA的混合溶液,HA的浓度大于0.2mol/L,根据物料守恒知,反应后的溶液中:c(A-)+c(HA)>0.1 mol/L,正确;D、根据题给数据②知,混合后溶液PH=7,c(OH-)=c(H+),结合电荷守恒,c(K+)+c(H+)=c(OH-)+c(A-),反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+),正确。
mol/L,错误;B、根据题给数据①知,0.1mol/L HA溶液和0.1mol/LKOH溶液等体积混合,恰好反应生成KA盐溶液,溶液PH常温下为9,说明溶液呈碱性,溶液中离子浓度大小为c(K+)>c(A-)>c(OH-)>c(H+),正确;C、根据题给数据②知,常温下混合后溶液PH=7,呈中性,则HA过量,溶液是HA和KA的混合溶液,HA的浓度大于0.2mol/L,根据物料守恒知,反应后的溶液中:c(A-)+c(HA)>0.1 mol/L,正确;D、根据题给数据②知,混合后溶液PH=7,c(OH-)=c(H+),结合电荷守恒,c(K+)+c(H+)=c(OH-)+c(A-),反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+),正确。
考点:考查电解质溶液中离子浓度大小比较。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案常温下,pH = 12的NaOH溶液与pH =1的HC1溶液按一定比例混合,所得溶液pH =2,则NaOH溶液与HC1溶液的体积比为
| A.9:2 | B.2:9 | C.1:9 | D.10:1 |
常温下,已知0.1mol·L-1的CH3COOH和HCN溶液的PH分别为a、b,且1<a< b。下列有关叙述不正确的是( )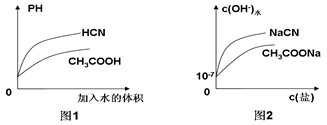
| A.常温下,等浓度的CH3COONa溶液和NaCN溶液的PH前者较小 |
| B.在NaCN溶液中:c (Na+)+ c (H+) =c (OH-)+ c (CN-) |
| C.相同温度下,相同PH的CH3COOH和HCN溶液分别加水稀释,溶液PH随溶液体积变化的曲线如图1所示 |
| D.常温下,CH3COONa溶液和NaCN溶液中由水电离出的c(OH-)与盐浓度的变化曲线如图2所示 |
下列叙述正确的是
| A.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
B.2SO2(g) + O2(g) 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 |
C.2NO+2CO 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 |
| D.25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小 |
下列物质的水溶液在适当加热时酸性增强的是
| A.氯化铁 | B.氯化钠 | C.盐酸 | D.碳酸钠 |
下列溶液一定呈中性的是( )
| A.c(H+)=c(OH-)=10-6mol/L溶液 | B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 | D.酸与碱恰好完全反应生成正盐的溶液 |
下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
| A.FeC13 | B.Ca(HCO3)2 | C.Na[Al (OH)4] | D.Na2SO3 |
下列比较中,正确的是
| A.等温等物质的量浓度溶液中,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大 |
| B.0.2 mol/L NH4Cl溶液和0.1 mol/LNaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)= c(S2-)+ c(HS-)+ c(H2S) |
| D.同浓度的下列溶液中:①NH4Al(SO4) 2②NH4Cl③CH3COONH4④NH3·H2O,c(NH4+)由大到小的顺序是①>②>③>④ |
在0.1 mol/L的Na2CO3溶液中,下列关系正确的是( )
A.c(Na+)=2c(CO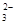 ) ) | B.c(OH-)=2c(H+) |
C.c(HCO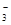 )>c(H2CO3) )>c(H2CO3) | D.c(Na+)<c(CO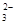 )+c(HCO )+c(HCO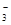 ) ) |