题目内容
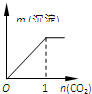
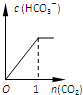
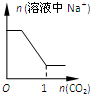
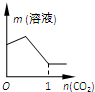
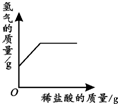
19.下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )| A | B | C | D |
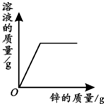
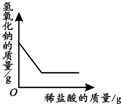
| 向一定量铁粉中滴加稀盐酸 | 向一定量硫酸铜溶液中不断加入锌粉 | 加热一定量高锰酸钾固体 | 向一定量氢氧化钠 溶液中滴加稀盐酸 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据通常情况下,铁和稀盐酸反应能生成氯化亚铁和氢气分析;
B、根据锌和硫酸铜反应能生成硫酸锌和铜分析;
C、根据高锰酸钾受热分解能生成锰酸钾、二氧化锰和氧气结合元素守恒分析;
D、根据氢氧化钠和盐酸发生中和反应来分析.
解答 解:A、在一定量的铁粉中加盐酸,生成氢气,随着反应的进行氢气由0逐渐增大,当铁粉全部反应完,反应停止,故A错误;
B、向一定量的硫酸铜溶液中加锌,反应刚开始溶液的质量起点不应该是0,故B错误;
C、加热高锰酸钾其中的锰元素都转化生成固体锰酸钾、二氧化锰中的锰,反应前后该元素质量不变,故C正确;
D、由题意可知,氢氧化钠溶液量一定,盐酸过量,所以随着反应的进行,氢氧化钠的质量最后变为0,故D错误;
故选:C.
点评 本题考查了根据图示中两种不同质量物质的反应或者一种物质反应情况来判断生成物、反应物的浓度、剩余物质等随时间或者某种反应物的变化关系;关键是弄清楚图中曲线的变化情况.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.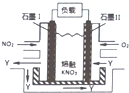 NO2、O2和熔融KNO3,可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法不正确的是( )
NO2、O2和熔融KNO3,可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法不正确的是( )
 NO2、O2和熔融KNO3,可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法不正确的是( )
NO2、O2和熔融KNO3,可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法不正确的是( )| A. | NO2在石墨I附近发生氧化反应 | |
| B. | 该电池放电时N03-向石墨I电极迁移 | |
| C. | 石墨Ⅱ附近发生的反应:O2+4e-+2N205=4 N03- | |
| D. | 相同条件下,放电过程中消耗的NO2和O2的体积比为l:4 |
7.空气的成分中,体积分数约占 78%的是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
14.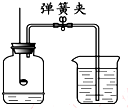 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )| A. | 实验时红磷一定过量 | |
| B. | 点燃红磷前先用弹簧夹夹紧乳胶管 | |
| C. | 红磷熄灭后立刻打开弹簧夹 | |
| D. | 最终进入瓶中水的体积约为氧气的体积 |
11.下列物质的转化在给定条件下能实现的是( )
| A. | H2SO4(稀)$→_{△}^{Cu}$SO2$\stackrel{少量氨水}{→}$NH4HSO3$\stackrel{足量氨水}{→}$(NH4)2SO3 | |
| B. | NH3$→_{催化剂△}^{O_{2}}$NO$\stackrel{O_{2}}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| C. | Fe$→_{△}^{少量Cl_{2}}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2$\stackrel{空气中放置}{→}$Fe(OH)3 | |
| D. | Al$\stackrel{NaOH溶液}{→}$NaAlO2$\stackrel{足量盐酸}{→}$AlCl3溶液$\stackrel{△}{→}$无水AlCl3 |
8.下列离子方程式书写正确的是( )
| A. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH2.H2O | |
| B. | 高锰酸钾酸性溶液吸收二氧化硫:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ | |
| C. | Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| D. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
9.下列说法正确的是( )
| A. | 地沟油和矿物油都属于酯类物质 | |
| B. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化 | |
| D. | 蛋白质、棉花、淀粉、油脂都是由高分子组成的物质 |