题目内容
1.X、Y、Z、W四种物质在一定条件下具有如图所示的转化关系,下列判断正确的是( )
| A. | 若图中反应均为非氧化还原反应,当W为一元强碱时,则X可能是NaAlO2 | |
| B. | 若图中反应均为非氧化还原反应,当W为一元强酸时,则X可能是NH3 | |
| C. | 若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2 | |
| D. | 若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl3 |
分析 由转化关系可知X可与W连续反应生成Y、Z,X也可与Z直接反应生成Y,
A.NaAlO2与NaOH不反应;
B.NH3与一元强酸反应生成铵盐;
C.如Z为CO2,W为非金属单质,X可为C,W为O2,Y为CO;
D.氯气与铁反应只生成FeCl3.
解答 解:由转化关系可知X可与W连续反应生成Y、Z,X也可与Z直接反应生成Y,
A.如X为NaAlO2,与NaOH不反应,故A错误;
B.如X为NH3,与一元强酸反应生成铵盐,只生成一种产物,Y与W不能再反应,故B错误;
C.如Z为CO2,W为非金属单质,X可为C,W为O2,Y为CO,故C正确;
D.如Z为FeCl3,W为金属单质,应为Fe,X为Cl2,但氯气与铁反应只生成FeCl3,Y不能为FeCl2,故D错误.
故选C.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注重掌握中学常见连续反应,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
11.下列实验操作与预期实验目的或所得实验结论都正确的是( )
| 编号 | 实验操作 | 实验目的或结论 |
| A | 向某有机物中加入新制Cu(OH)2悬浊液并加热,有砖红色沉淀 | 该有机物一定是醛 |
| B | 将CH3CH2Br与NaOH溶液混合加热,再滴加AgNO3溶液,未产生浅黄色沉淀 | 证明CH3CH2Br未发生水解 |
| C | 分别给乙醇和苯酚溶液中加入紫色石蕊试液,观察其颜色的变化 | 比较乙醇和苯酚的酸性强弱 |
| D | 用pH试纸测定CH3COONa溶液的pH | 证明CH3COOH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
12.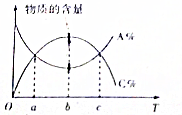 对于反应mA+nB?pC,在其它条件不变时,A与C两物质的物质的量随温度的变化情况如图所示,则下列说法正确的是( )
对于反应mA+nB?pC,在其它条件不变时,A与C两物质的物质的量随温度的变化情况如图所示,则下列说法正确的是( )
 对于反应mA+nB?pC,在其它条件不变时,A与C两物质的物质的量随温度的变化情况如图所示,则下列说法正确的是( )
对于反应mA+nB?pC,在其它条件不变时,A与C两物质的物质的量随温度的变化情况如图所示,则下列说法正确的是( )| A. | 该反应为吸热反应 | |
| B. | 在a,c时刻,正逆反应速率相等 | |
| C. | 若横轴为压强,则存在m+n<p | |
| D. | b时刻正逆反应速率大于c时刻的正逆反应速率 |
9.为实现下列实验目的,如表提供的主要仪器以及所用试剂均合理的是( )
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 配制480mL 2mol/L的NaOH溶液 | 胶头滴管、烧杯、玻璃棒、托盘天平、480mL容量瓶 | NaOH固体、蒸馏水 |
| B | 测定中和热 | 烧杯、玻璃棒、纸板、保温塑料、温度计 | 50mL0.5mol/LNaOH溶液与50mL0.5mol/L盐酸 |
| C | 测定生成H2速率 | 分液漏斗、锥形瓶、针筒、铁架台 | Zn粒、稀硫酸 |
| D | 浓硫酸脱水性 | 分液漏斗、试管 | 蔗糖 |
| A. | A | B. | B | C. | C | D. | D |
13.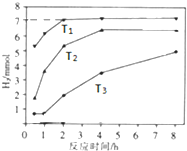 在一定温度下,向容积为2L的密闭容器中加入1mol A和2mol B,发生如下反应:A(g)+2B(g)?2C(g)△H,经5min达到平衡时,生成0.4mol C,下列叙述中正确的是( )
在一定温度下,向容积为2L的密闭容器中加入1mol A和2mol B,发生如下反应:A(g)+2B(g)?2C(g)△H,经5min达到平衡时,生成0.4mol C,下列叙述中正确的是( )
 在一定温度下,向容积为2L的密闭容器中加入1mol A和2mol B,发生如下反应:A(g)+2B(g)?2C(g)△H,经5min达到平衡时,生成0.4mol C,下列叙述中正确的是( )
在一定温度下,向容积为2L的密闭容器中加入1mol A和2mol B,发生如下反应:A(g)+2B(g)?2C(g)△H,经5min达到平衡时,生成0.4mol C,下列叙述中正确的是( )| A. | 反应的平均速率v(A)=0.04 mol/(L•min) | |
| B. | 达平衡时A、B的转化率相等 | |
| C. | 向平衡混合物中再加入0.1 mol A、0.2 mol B,达新平衡时C的体积分数减小 | |
| D. | 若升高温度达新平衡后,A的浓度增大,则△H>0 |
10.常温离子液体也称常温熔融盐,硝酸乙基铵[(C2H5NH3)NO3]是人类发现的第一种常温离子液体,其熔点为12℃.已知C2H5NH2的化学性质与NH3相似,C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是( )
| A. | 硝酸乙基铵水溶液呈碱性 | |
| B. | 该离子液体可以作为电池的电解质 | |
| C. | (C2H5NH3)NO3能与氢氧化钠反应产生NH3 | |
| D. | 相同温度下,相同物质的量的浓度的硝酸乙基铵溶液和硝酸铵溶液相比前者的pH小 |
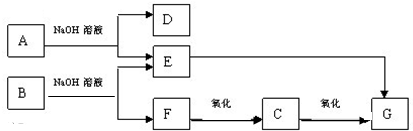

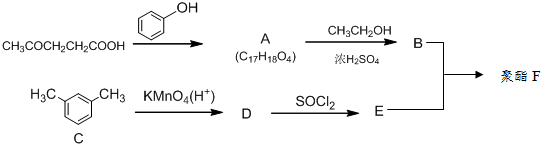
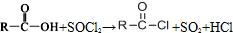 ②
② (R、R′表示烃基)
(R、R′表示烃基)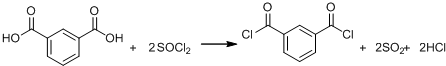
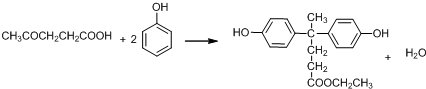
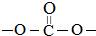 结构.
结构.