题目内容
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、1.8g NH4+中含有的质子数为NA |
| B、标准状况下,2.24L CO2和SO2混合气中氧原子数为0.1NA |
| C、12g Mg与足量盐酸反应时,失去的电子数为NA |
| D、100mL 1mol?L-1的醋酸溶液中,CH3COO-离子数为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铵根离子中含有11个质子,1.8g铵根离子的物质的量为0.1mol,含有1.1mol质子;
B.二氧化碳和二氧化硫中都含有两个氧原子,0.1mol混合气体中含有0.2mol氧原子;
C.镁为2价金属,12g镁的物质的量为0.5mol,0.5mol镁完全反应失去1mol电子;
D.醋酸为弱电解质,溶液中部分电离出醋酸根离子.
B.二氧化碳和二氧化硫中都含有两个氧原子,0.1mol混合气体中含有0.2mol氧原子;
C.镁为2价金属,12g镁的物质的量为0.5mol,0.5mol镁完全反应失去1mol电子;
D.醋酸为弱电解质,溶液中部分电离出醋酸根离子.
解答:
解:A.1.8g铵根离子的物质的量为0.1mol,0.1mol铵根离子中含有1.1mol质子,含有的质子数为1.1NA,故A错误;
B.标准状况下,2.24L混合气体的物质的量为0.1mol,0.1mol二氧化碳和二氧化硫的混合气体中含有0.2mol氧原子,含有氧原子数为0.2NA,故B错误;
C.12g镁的物质的量为0.5mol,0.5mol镁与足量稀盐酸反应生成0.5mol氢气,失去了1mol电子,失去的电子数为NA,故C正确;
D.100mL 1mol?L-1的醋酸溶液中含有醋酸0.1mol,醋酸为弱酸,只能部分电离出醋酸根离子,则溶液中的醋酸根离子小于0.1mol,CH3COO-离子数小于0.1NA,故D错误;
故选C.
B.标准状况下,2.24L混合气体的物质的量为0.1mol,0.1mol二氧化碳和二氧化硫的混合气体中含有0.2mol氧原子,含有氧原子数为0.2NA,故B错误;
C.12g镁的物质的量为0.5mol,0.5mol镁与足量稀盐酸反应生成0.5mol氢气,失去了1mol电子,失去的电子数为NA,故C正确;
D.100mL 1mol?L-1的醋酸溶液中含有醋酸0.1mol,醋酸为弱酸,只能部分电离出醋酸根离子,则溶液中的醋酸根离子小于0.1mol,CH3COO-离子数小于0.1NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项A为易错点,注意题中计算的是质子数,不是电子数.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁 |
| D、制钛:用金属钠置换TiCl4溶液中的钛 |
下列反应的离子方程式书写正确的是( )
| A、FeS固体溶于稀HNO3:FeS+2H+=Fe2++H2S↑ |
| B、AlCl3和过量氨水反应:Al3++3OH-=Al(OH)3↓ |
| C、向AgCl悬浊液中滴加硫化钠溶液,白色沉淀变成黑色:2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-(aq) |
| D、体积等浓度的NaHSO4与Ba(0H)2溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
下列表达方式错误的是( )
| A、HCl的电子式 H:Cl |
B、S2-的结构示意图是: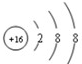 |
| C、O-18原子的符号:818O |
| D、CO2分子的结构式 O=C=O |
下列关于氯的说法正确的是( )
| A、Cl2在化学反应中既能作氧化剂,又能作还原剂 |
| B、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| C、Cl2通入到含有酚酞的NaOH溶液中,红色褪去,因为氯气有漂白性 |
| D、将SO2通入次氯酸钙溶液可生成次氯酸 |
下列说法正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D、相同条件下,溶液中Cu2+、Fe3+、Zn2+的氧化性依次增强 |
常温下,Na2CO3溶液中有平衡CO32-+H2O?HCO3-+OH-( )
| A、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(H+) |
| B、加入NaOH固体,溶液pH减小 |
| C、Na2CO3溶液中:c(Na+)+c(H+)═2c(CO32-)+c(OH-) |
| D、升高温度平衡向正反应方向移动 |
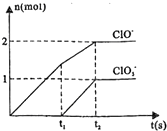 已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.
已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示. 已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )