题目内容
16.下列叙述中,正确的是( )| A. | 乙醛与银氨溶液水浴共热,发生还原反应得到光亮如镜的银 | |
| B. | 苯乙烯与氢气在合适条件下,发生加成反应生成乙基环己烷 | |
| C. | 乙醇与浓硫酸共热迅速升温至140℃时,发生消去反应生成乙烯 | |
| D. | 甲苯与氯气在光照下,发生取代反应主要生成2,4二氯甲苯 |
分析 A.乙醛被氧化;
B.苯乙烯含有碳碳双键和苯环,都可发生加成反应;
C.乙醇发生消去反应时应加热到170℃;
D.光照时,取代甲基中的氢原子.
解答 解:A.乙醛与银氨溶液水浴共热,乙醛被氧化生成乙酸,故A错误;
B.苯乙烯含有碳碳双键和苯环,都可发生加成反应,最终产物为乙基环己烷,故B正确;
C.乙醇发生消去反应时应加热到170℃,加热至140℃时生成乙醚,故C错误;
D.反应条件不同产物不同,光照时,取代甲基中的氢原子,在催化作用下苯环上的氢原子被取代,故D错误.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的性质以及反应条件,有机反应要严格控制反应条件,否则易生成副产物,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.在温度t℃下,某Ba(OH)2的稀溶液中?c(H+)=10-amol.L-1,c(OH-)=10-b mol.L-1,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
(1)依据题意判断,t℃大于25℃(填”大于”“小于”或”等于”),该温度下水的离子积KW=1×10-12.
(2)b=4,原Ba(OH)2的稀溶液的物质的量浓度为?5×10-5mol/L?.
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为4,以及其中Na2SO4的物质的量浓度为1×10-4mol/L.
| 序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
(2)b=4,原Ba(OH)2的稀溶液的物质的量浓度为?5×10-5mol/L?.
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为4,以及其中Na2SO4的物质的量浓度为1×10-4mol/L.
11.锌-溴蓄电池的充、放电的电池总反应为Zn+Br2$?_{充电}^{放电}$Zn2++2Br-,下列各反应:①Zn-2e-=Zn2+;②Br2+2e-=2Br-;③2Br--2e-=Br2;④Zn2++2e-=Zn,其中充电的阳极和放电的负极的反应分别是( )
| A. | ①② | B. | ③② | C. | ④② | D. | ③① |
1.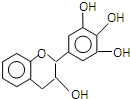 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A. | 1 molEGC与足量溴水反应可消耗2 mol Br2 | |
| B. | EGC与苯酚属于同系物 | |
| C. | 在一定条件下,EGC中的羟基可被氯原子取代生成氯代烃 | |
| D. | 1mol EGC与含1.5mol Na2CO3的水溶液恰好完全反应生成1.5molCO2 |
5.如图是金属晶体的面心立方最密堆积方式的晶胞示意图,在密堆积中处于同一密层上的原子组合是( )
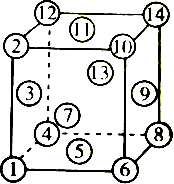

| A. | ④⑤⑥⑩⑪⑫ | B. | ②③④⑤⑥⑦ | C. | ①④⑤⑥⑧ | D. | ①②⑪⑭⑧⑤ |
20.用式量是57的烃基取代甲苯苯环上的一个氢原子,能得到的有机物种数为( )
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 24种 |
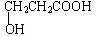 ,该物质易溶于水(填“难”或“易”),原因是能与水分子形成氢键,该物质的熔点明显高于相对分子质量相接近的烃类化合物的熔点,原因是该物质分子间可形成氢键.
,该物质易溶于水(填“难”或“易”),原因是能与水分子形成氢键,该物质的熔点明显高于相对分子质量相接近的烃类化合物的熔点,原因是该物质分子间可形成氢键.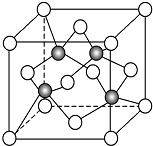 碳及其化合物与人类关系密切
碳及其化合物与人类关系密切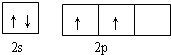 ,C、N、O三元素的第一电离能由大到小的顺序为N>O>C,在丙烯分子中碳原子的杂化方式为sp2、sp3.
,C、N、O三元素的第一电离能由大到小的顺序为N>O>C,在丙烯分子中碳原子的杂化方式为sp2、sp3.