��Ŀ����
����Ŀ��ȼú�����к���һ�����Ķ���������ɴ�����Ⱦ��һ�������£�ͨ�����з�Ӧ����ʵ��ȼú��������Ļ��գ�2CO��g��+SO2��g��![]() 2CO2��g��+S��l�� H�� ��ش�
2CO2��g��+S��l�� H�� ��ش�
����֪CO��g��+![]() O2��g��=CO2��g�� ��H1=-a kJ��mol-1
O2��g��=CO2��g�� ��H1=-a kJ��mol-1
S��s��+O2��g��=SO2��g�� H2=-b kJ��mol-1
S��l��=S��s�� H3=-c kJ��mol-1
����H=_______kJ��mol-1��
��һ���¶��£���2L�����ܱ�������ͨ��2molCO��1molSO2���ڲ�ͬ�����½��з�Ӧ��2CO��g��+SO2��g��![]() 2CO2��g��+S��l������Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��
2CO2��g��+S��l������Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��
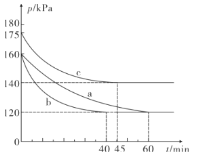
��ͼ������ʵ��ӷ�Ӧ��ʼ���ﵽƽ��ʱ�ķ�Ӧ����v��CO���ɴ�С�Ĵ���Ϊ___�� ��ʵ����ţ��� ��a����ȣ�c��ı��ʵ������������___��
����b�鷴Ӧ���е�40minʱ�ﵽƽ��״̬����ʱ���������������ܶȱȷ�Ӧǰ������12.8 g��L-1����CO�����ʵ���Ũ��c��CO��=___����Ӧ�ڴ������µĻ�ѧƽ�ⳣ��K=___
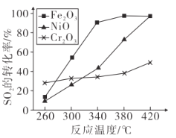
������������ͬ��������ͬʱ��SO����ת�����淴Ӧ�¶ȵı仯����ͼ��260��Cʱ��______����Fe2O3��NiO��Cr2O3����������Ӧ������죻Fe2O3��NiO��������ʹSO2��ת���ʴﵽ��ߣ������Ǽ۸����أ�ѡ��Fe2O3����Ҫ�ŵ���_______��
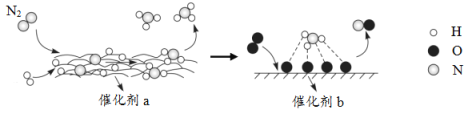
��SO2��O2���ӽ���Ĥȼ�ϵ��ʵ���������ᡢ���硢��������Ŀ�꣬�˵�صĸ�����ӦʽΪ____________��
���𰸡�b+c-2a b>c>a �����¶� 0.2mol��L-1 160 Cr2O3 ����Խϵ͵��¶��¿ɻ�ýϸߵ�SO2��ת���ʣ��Ӷ���Լ������Դ SO2+2H2O-2e-=SO42-+4H+
��������
���ݸ�˹���ɿ�֪����H����ͨ����H1��=2-H2-H3�õ���2CO��g��+SO2��g��![]() 2CO2��g��+S��l��Ϊ��Ӧǰ�������������С�ķ�Ӧ�����⣨2��ͼ�����߹յ��֪��b���ȴﵽƽ�⣬���Ϊa�飻SO2��O2���ӽ���Ĥȼ�ϵ����SO2ͨ�븺����O2ͨ��������
2CO2��g��+S��l��Ϊ��Ӧǰ�������������С�ķ�Ӧ�����⣨2��ͼ�����߹յ��֪��b���ȴﵽƽ�⣬���Ϊa�飻SO2��O2���ӽ���Ĥȼ�ϵ����SO2ͨ�븺����O2ͨ��������
��1����CO��g��+![]() O2��g��=CO2��g�����Ϊ�٣�S��s��+O2��g��=SO2��g�����Ϊ�ڣ�S��l��=S��s�����Ϊ�ۣ���Ӧ2CO��g��+SO2��g��
O2��g��=CO2��g�����Ϊ�٣�S��s��+O2��g��=SO2��g�����Ϊ�ڣ�S��l��=S��s�����Ϊ�ۣ���Ӧ2CO��g��+SO2��g��![]() 2CO2��g��+S��l�����ɢ���2-��-�۵õ������ݸ�˹���ɣ���H=2����H1-H2-H3==��-2a +b+c��kJ��mol-1��
2CO2��g��+S��l�����ɢ���2-��-�۵õ������ݸ�˹���ɣ���H=2����H1-H2-H3==��-2a +b+c��kJ��mol-1��
��2�������⣨2��ͼ�����߹յ��֪��b���ȴﵽƽ�⣬���Ϊa�飬�ʷ�Ӧ����v��CO���ɴ�С�Ĵ���Ϊb>c>a��
�ڷ�Ӧ�ﵽƽ��״̬����ʱ���������������ܶȱȷ�Ӧǰ������12.8 g��L-1�����ٵ�����������ΪS��l����������m=12.8 g��L-1��2L=25.6g��n=![]() �����ݷ�Ӧ����ʽ��֪�����뷴Ӧ��һ����̼�����ʵ���Ϊn(CO)=1.6mol��ʣ���һ����̼�����ʵ���Ϊ0.4mol����CO�����ʵ���Ũ��c��CO��=0.2mol��L-1��c(CO2)=0.8 mol��L-1��n(SO2)=0.1 mol��L-1����ѧƽ�ⳣ��K=
�����ݷ�Ӧ����ʽ��֪�����뷴Ӧ��һ����̼�����ʵ���Ϊn(CO)=1.6mol��ʣ���һ����̼�����ʵ���Ϊ0.4mol����CO�����ʵ���Ũ��c��CO��=0.2mol��L-1��c(CO2)=0.8 mol��L-1��n(SO2)=0.1 mol��L-1����ѧƽ�ⳣ��K=![]() ��
��
��3��260��Cʱ����ͬʱ���ڼ���Cr2O3��SO2ת������ߣ���Ϊ�¶���ͬ��������Ӱ��ƽ�⣬���Լ���Cr2O3���ﵽƽ�⣻������ͼ�п�֪Fe2O3������ʱ������Խϵ��¶ȿɻ�ýϸߵ�SO2��ת���ʣ��Ӷ���Լ������Դ��
��4��SO2�ڸ���ʧ���ӷ�Ӧ������Ӧ�������ᣬ�缫��ӦʽΪSO2+2H2O-2e-=SO42-+4H+��

����Ŀ��HClO4��H2SO4��HNO3��HCl����ǿ�ᣬ���ǵ�������ˮ��Һ�в��������ij�¶������������ڱ������еĵ��볣����
�� | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6��10��5 | 6.3��10��9 | 1.6��10��9 | 4.2��10��10 |
����˵���в���ȷ����(����)
A.�ڱ��������������ᶼû����ȫ����
B.�ڱ�������HClO4��������������ǿ����
C.�ڱ�������H2SO4�ĵ��뷽��ʽΪH2SO4===2H����SO![]()
D.ˮ�����������������ǿ����������������������������ǿ��
����Ŀ����ѧ������(chemical oxygen demand�����COD)��ʾ��ǿ�����������ظ�������� 1 L ��ˮ���л���������������������������������Ϊ������ʱ��1 Lˮ��������O2������(mg��L-1)���㡣CODС��ˮ�ʺá�ij������ֳೱ��ij��ѧ��ȤС��Ϊ�ⶨ����Ⱦ�̶ȣ��� 1.176 g K2Cr2O7�������Ƴ� 100 mL��Һ����ȡˮ��20.00 mL������10.00 mL K2Cr2O7��Һ��������������ʹ��������ȷ�Ӧ2 h�������K2Cr2O7��0.100 0 mol��L-1Fe(NH4)2(SO4)2��Һ���еζ�������Fe(NH4)2(SO4)2��Һ��������±���ʾ����ʱ�������ķ�Ӧ��CrO72-+6Fe2��+14H+=2Cr3��+6Fe3++7H2O��(��֪K2Cr2O7���л��ﷴӦʱ����ԭΪ Cr3+��K2Cr2O7����Է�������Ϊ294)
��� | ��ʼ����/mL | �յ����/mL |
1 | 0.00 | 12.10 |
2 | 1.26 | 13.16 |
3 | 1.54 | 14.64 |
(1)K2Cr2O7��Һ�����ʵ���Ũ��Ϊ______mol��L-1��
(2)��ú�ˮ��CODΪ______mg��L-1��