题目内容
25℃时,在1.0 L浓度均为0.01 mol·L-1的某一元酸HA与其钠盐组成的混合溶液中,测得c(Na+)>c(A-),则下列描述中,不正确的是
A.该溶液的pH<7
B.HA的酸性很弱,A-水解程度较大
C.c(A-)+c(HA)="0.02" mol·L-1
D.n(A-)+n(OH-)=0.01 mo1+n(H+)
A
解析试题分析:等浓度的HA和NaA形成混合溶液,若c(Na+)>c(A-),说明A-的水解大于HA的电离,溶液呈碱性,因此A错误,B正确;C、根据元素守恒,A元素的总浓度为0.02 mol·L-1,正确;D、根据电荷守恒,n(A-)+n(OH-)=n(Na+)+n(H+),n(Na+)="0.01" mo1,正确。
考点:考查了溶液中守恒关系和溶液电离水解的相关知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
25℃时,0.01 mol·L-1两种弱酸溶液的pH如表,下列说法正确的是
| A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大 |
| B.物质的量浓度相同的CH3COONa与NaCN 溶液中,CH3COONa溶液pH较大 |
| C.等体积pH相同的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH |
| D.HCN的电离平衡常数(Ka)与CN—的水解平衡常数(K)存在如下关系:Ka?K=Kw |
已知:H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8;H2CO3的Ka1=4.2×10-7,Ka 2=5.6×10-11。现将标准状况下2.24L的CO2和2.24L的SO2分别通入两份150mL1mol/LNaOH溶液中,关于两溶液的比较下列说法正确的是
| A.c(HCO3-)<c(CO32-) |
| B.两溶液都能使酸性高锰酸钾溶液褪色 |
| C.c(HCO3-)>c(HSO3-) |
| D.c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(CH3COO-)+c(OH-) |
| B.物质的量浓度相等CH3COOH和CH3COONa混合溶液: c(CH3COO-)-c(CH3COOH)=2 c(H+)-2 c(OH-) |
C.CH3COOH溶液加水稀释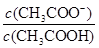 不变 不变 |
D.CH3COOH溶液加水稀释,溶液中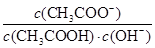 不变 不变 |
下列关于难溶电解质溶液说法正确的是 ( )
| A.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| B.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
| C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl- |
| D.25 ℃时,在Mg(OH)2悬浊液中加入少量的NH4Cl固体后,c(Mg2+)增大 |
下列说法中正确的是
A.若M度T0C时水的离子积常数为KW在该温度下的中性溶液中c(H+)= mol/L mol/L |
| B.25℃时HCl溶液中的c(H+)一定大于25℃时NH4Cl溶液中的c(H+) |
| C.1mol/LCH3COOH溶液和1mol ? L-1KOH溶液等体积混合,混合溶液中c(K+)=c(CH3COO-) |
| D.pH =5.7的 NaHSO3溶液中:c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-) |
等浓度的NaOH溶液与氢硫酸溶液反应,下列说法不正确的是
| A.溶液中始终有:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| B.溶液呈中性时:c(Na+)=c(HS-)+c(S2-) |
| C.等体积混合后溶液中一定有:c(H2S)+c(H+)=c(S2-)+c(OH-) |
| D.恰好完全中和后的溶液中:c(Na+)>2c(S2-) |
在V mL 0.1 mol/L Na2S溶液中逐滴加入V mL 0. 1 mol/L KHSO4溶液,所得溶液中粒子浓度关系正确的是
| A.c(SO42-)= c(HS-) =c(K+) >c(OH-)=c(H+) |
| B.c(Na+)> c(K+)> c(S2-)> c(H+)>c(OH-) |
| C.c(Na+)= c(S2-)+ c(H2S)+c(HS-)+ c(SO42-) |
| D.c(K+)+ c(Na+)+ c(H+)= c(SO42-)+ c(S2-)+ c(HS-)+ c(OH-) |