题目内容
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+1、+2等,故能形成多种铜的化合物。
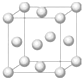
(1)基态铜原子的电子排布式是____________;铜晶体晶胞结构如图所示,该晶胞实际拥有________ 个铜原子;该种堆积方式______(填“是”或“不是”)密置堆积。
(1)基态铜原子的电子排布式是____________;铜晶体晶胞结构如图所示,该晶胞实际拥有________ 个铜原子;该种堆积方式______(填“是”或“不是”)密置堆积。

(2)许多+1价铜的配合物溶液能吸收CO和烯烃(如C2H4、CH3CH=CH2等)。试问,形成配合物的条件是________________ ,已知CO和N2属于等电子体,试写出CO的结构式______________,CH3CH=CH2分子中碳原子采取的杂化方式有________________。
(3)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,后沉淀溶解形成深蓝色的溶液。写出蓝色沉淀溶解的离子方程式__________________________;根据价层电子对互斥理论,预测SO42-的空间构型为___________,与SO42-互为等电子体的原子团有____________ (试写两例)。
(3)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,后沉淀溶解形成深蓝色的溶液。写出蓝色沉淀溶解的离子方程式__________________________;根据价层电子对互斥理论,预测SO42-的空间构型为___________,与SO42-互为等电子体的原子团有____________ (试写两例)。
(1)1s22s22p63s23p63d104s1或[Ar]3d104s1;4;是
(2)中心离子有空轨道,配体有孤电子对;C O;Sp2 、sp3
O;Sp2 、sp3
(3)Cu(OH)2+4NH3 = [Cu(NH3)4]2++2OH-;正四面体;PO43-、ClO4-
(2)中心离子有空轨道,配体有孤电子对;C
 O;Sp2 、sp3
O;Sp2 、sp3(3)Cu(OH)2+4NH3 = [Cu(NH3)4]2++2OH-;正四面体;PO43-、ClO4-

练习册系列答案
相关题目
 铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+1、+2 等,故能形成多种铜的化合物.
铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+1、+2 等,故能形成多种铜的化合物. [化学--物质结构与性质]
[化学--物质结构与性质]