题目内容
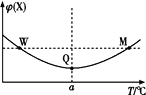
【题目】25℃时,向25ml氢氧化钠标准溶液中逐滴加入0.2mol·L1的一元酸HA溶液,PH变化曲线如下图所示:

(1)该氢氧化钠溶液的物质的量浓度为__________mol·L1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH)= _______mol·L1。
(3)HA是____酸(选填“强”、“弱”)。
(4) 在B点所得混合溶液中,c(Na+)、c(A)、c(H+)、c(OH) 的大小的顺序是_____________。
(5)在C点所得混合溶液中,下列说正确的是________。
A.HA的电离程度小于NaA的水解程度
B.离子浓度由大到小的顺序是c(Na+)>c(A)>c(H+)>c(OH)
C.c(Na+) + c(H+) = c(A-) + c(OH)
D.c(HA) + c(A) = 0.2mol·L1
【答案】0.1 1.0×10-4 弱 c(Na+)=c(A)>c(H+)=c(OH) C
【解析】
(1)NaOH为强碱,由图像可知,其pH=13;
(2)A点对应酸的体积为12.5mL,恰好反应生成NaA,为强碱弱酸盐,水解呈碱性;
(3)NaA溶液呈碱性;
(4)B点溶液呈中性;
(5)A.C点时,n(HA)=2n(NaOH),溶液呈酸性;
B.HA过量,结合电荷守恒判断;
C.根据电荷守恒判断;
D.C点时溶液体积为50mL,为HA溶液体积的2倍。
(1)NaOH为强碱,其pH=13,氢氧化钠溶液的物质的量浓度为0.1mol/L;
(2)A点对应酸的体积为12.5mL,恰好反应生成NaA,为强碱弱酸盐,水解呈碱性,促进水的电离,此时pH=10,则c(OH-)=1×10-4 molL-1;
(3)由(2)可知NaA溶液呈碱性,则HA为弱酸;
(4)溶液中存在电荷守恒:c(Na+)+ c(H+)=c(A-)+ c(OH-),B点溶液呈中性,则溶液中存在c(Na+)=c(A-)>c(H+)=c(OH-);
(5)A.C点时,n(HA)=2n(NaOH),溶液呈酸性,则HA的电离程度大于NaA的水解程度,故A错误;
B.HA过量,溶液呈酸性,则c(H+)>c(OH-),又因c(Na+)+c(H+)=c(A-)+c(OH-),则c(A-)>c(Na+),故B错误;
C.溶液存在电荷守恒,则c(Na+)+c(H+)=c(A-)+c(OH-),故C正确;
D.C点时溶液体积为50mL,为HA溶液体积的2倍,则c(HA)+c(A-)=0.1molL-1,故D错误;
故答案为:C。

 53天天练系列答案
53天天练系列答案