题目内容
(18分)钛被誉为“二十一世纪的金属”,用途广泛。按下图所示组成的产业链可以大大提高资源利用率并能减少环境污染。请回答下列问题:
(1)已知中FeTiO3元素的化合价为+3,钛铁矿经氯化法得到四氯化钛的过程中________元素被氧化,每生产1. 9kgTiCl4消耗Cl2在标准状况下的体积为________L。
则金属Mg还原TiCl4制取金属Ti (s)的热化学方程式为___________.
(3)某化学兴趣小组探究外界条件对合成甲醇反应的影响。
①在300℃时,向体积为1L的密闭容器中加入2mol H2和1mol CO,CO和CH3OH(g)的浓度随时间变化如图所示。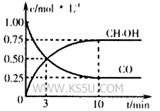
则从反应开始到建立平衡,v(H2)为___________ ;
该温度下 的化学平衡常
的化学平衡常
数为___________ 。
。
②在其它条件不变,只改变其中的一个条件,该小组同学
根据实验绘制如下图像,其中与事实相符的是为___________(填
序号)。
(4)电解饱和食盐水是氯碱工业的基础。
①电解饱和食盐水的离子方程式为为___________ 。
②电解时用盐酸控制阳极区溶液的pH在2~3,盐酸的作用为为___________。(用必要的离子方程式和文字说明)
(18分)
(1)Ti、C(2分),784(3分)
(2)2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s) ?H=-478kJ?mol?1(2分)
(3)①0.15mo?L-1?min-1(2分) 12(2分)
②AD(3分)(缺1项扣1分,有错误选项不给分)
(4)①2Cl?+2H2O  H2↑+Cl2↑+2OH?(2分)
H2↑+Cl2↑+2OH?(2分)
②Cl2与H2O反应:Cl2+H2O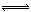 H++Cl?+HClO,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。(2分)
H++Cl?+HClO,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。(2分)
解析试题分析:(1)根据流程图可知FeTiO3、C、Cl2反应生成FeCl3、TiCl4、CO,化合价升高的元素为Ti和C,所以Ti和C元素被氧化;1. 9kgTiCl4消物质的量为:1900g÷190g/mol=10mol,根据FeTiO3可知生成的FeCl3和TiCl4物质的量相等,都是10mol,根据Cl元素守恒Cl2的物质的量为(30mol+40mol)÷2=35mol,所以消耗Cl2在标准状况下的体积为:35mol×22.4L/mol=784L。
(2)首先写出金属Mg还原TiCl4制取金属Ti (s)的化学方程式,并注明状态:2Mg(s)+TiCl4(g)=2MgCl2(s)+
Ti(s),然后根据盖斯定律求焓变,?H=2?H1—?H2=-478kJ?mol?1,可得热化学方程式。
(3)①v(H2)=v(CH3OH)=2×0.75mol/L÷10min=0.15mo?L-1?min-1;根据三段式进行计算:
CO(g) + 2H2(g) 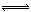 CH3OH(g)
CH3OH(g)
起始浓度(mol?L?1) 1 2 0
转化浓度(mol?L?1) 0.75 1.5 0.75
平衡浓度(mol?L?1) 0.25 0.5 0.75
则化学平衡常数为:0.75mol/L÷[0.25mol/L×(0.5mol/L )2] =12(mol?L?1)-2
② A、CO与H2生成CH3OH的反应为放热反应,350℃大于300℃,反应速率加快,平衡向逆反应方向移动,甲醇的物质的量减小,正确;B、该反应正反应方向气体系数减小,所以增大压强平衡向右移动,甲醇的物质的量增大,图像错误;C、该反应为放热反应,350℃大于300℃,反应速率加快,平衡向逆反应方向移动,甲醇的物质的量减小,图像错误;D、催化剂能加快反应速率,但不影响化学平衡,图像正确。
(4)①电解饱和食盐水生成H2、Cl2、NaOH,离子方程式为:2Cl?+2H2O  H2↑+Cl2↑+2OH?
H2↑+Cl2↑+2OH?
②因为阳极生成Cl2,Cl2能溶于H2O且与水反应:Cl2+H2O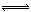 H++Cl?+HClO,加入盐酸控制阳极区溶液的pH在2~3,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。
H++Cl?+HClO,加入盐酸控制阳极区溶液的pH在2~3,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。
考点:本题考查热化学方程式书写、化学反应速率与化学平衡、电解原理、化学计算。

一定温度下,向1.0L密闭容器中加入0.60molX(g),发生反应X(g)  Y(s)+2Z(g)△H>0测得反应物X浓度与反应时间的数据如下表
Y(s)+2Z(g)△H>0测得反应物X浓度与反应时间的数据如下表
| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/(mol·L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)3min时用Z表示的平均反应速率v(Z)= 。
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是 。由此规律推出反应在6min时反应物的浓度a为 mol·L-1。
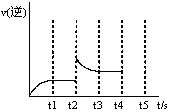
(3)反应的逆反应速率随时间变化的关系如图,t2时改变了某一种条件,改变的条件可能是 、 (填写两顶)
(4)下列哪些情况表明容器中已达平衡状态 (填字母序号)
A.容器体积一定时气体密度不再变化
B.反应的平衡常数不再变化
C.容器中气体的平均相对分子质量不随时间而变化
D.Y的物质的量不再发生变化
E.Z的生成速率等于X的消耗速率的2倍
(16分)高铁酸钠(Na2FeO4)具有很强的氧化性,广泛应用于净水、电池工业等领域。以粗FeO(含有CuO、Al2O3和SiO2等杂质)制备高铁酸钠的生产流程如下,回答下列问题: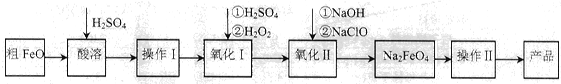
已知:NaClO不稳定,受热易分解。
(1)粗FeO酸溶过程中通入水蒸气(高温),其目的是__________________________。
(2)操作I目的是得到高纯度FeSO4溶液,则氧化I中反应的离子方程式为_________。
(3)本工艺中需要高浓度NaClO溶液,可用Cl2与NaOH溶液反应制备
①Cl2与NaOH溶液反应的离子方程式为_________________。
②在不同温度下进行该反应,反应相同一段时间后,测得生成NaClO浓度如下:
| 温度/℃ | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO浓度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |
其原因为____________________________________________________________________。
(4)工业也常用电解法制备Na2FeO4,其原理为Fe+2OH-+2H2O电解FeO42-+3H2↑。请用下列材料设计电解池并在答题卡的方框内画出该装置。

可选材料:铁片、铜片、碳棒、浓NaOH溶液、浓HCl等
其阳极反应式为:________________________________。
硫酸工业在国民经济中占有极其重要的地位。请回答硫酸工业中的如下问题:
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在 郊
区(填标号);
| A.有丰富黄铁矿资源的城市 | B.风光秀丽的旅游城市 |
| C.消耗硫酸甚多的工业城市 | D.人口稠密的文化、商业中心城市 |
该反应的化学方程式为 。
(3)为提高SO3吸收率,实际生产中通常用 吸收SO3。
(4)已知反应2SO2+O2
 SO3 △H <0,现将0.050mol SO2和0.030mol O2
SO3 △H <0,现将0.050mol SO2和0.030mol O2充入容积为1L的密闭容器中,反应在一定条件下达到平衡,测得反应后容器压
强缩小到原来压强的75%,则该条件下SO2的转化率为________;该条件下的
平衡常数为__________。
(5)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在
沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 炉渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
温度升高而降低的原因 。
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方
法可用 (填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产
水泥的辅料,写出这两步反应的化学方程式 。
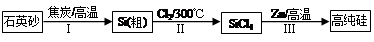
 Si(S)+2ZnCl2(l) △H1<0
Si(S)+2ZnCl2(l) △H1<0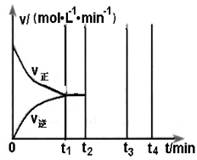
 2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC。又知在此时D的平均速率为0.15 mol·L-1·min-1。
2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC。又知在此时D的平均速率为0.15 mol·L-1·min-1。