题目内容
2.在 pH=9的氢氧化钠和 pH=9 的醋酸钠的两种溶液中,假设由水电离出的氢氧根离子的物质的量浓度分别为 Amol•L-1和Bmol•L-1,则A和B的关系是( )| A. | A=1×10-4B | B. | B=1×10-4A | C. | A>B | D. | A=B |
分析 依据溶液pH计算氢离子浓度,结合盐类水解特征和溶液中离子积常数计算分析判断,水本身电离出的氢离子和氢氧根离子浓度相同.
解答 解:设pH=9的氢氧化钠和醋酸钠两种溶液中由水电离产生的[OH-]为A mol•L-1和B mol•L-1,pH=9的氢氧化钠溶液中c(H+)水=c(OH-)水=10-9mol/L,醋酸钠溶液中,醋酸根离子水解生成醋酸和氢氧根离子,pH=9的醋酸钠溶液中c(H+)=10-9mol/L,则水电离出c(OH-)水=$\frac{1{0}^{-14}}{1{0}^{-9}}$=10-5mol/L,水电离出则A与B的关系是:A:B=10-9mol/L:10-5mol/L,A=10-4B;故选A.
点评 本题考查了盐类水解分析,溶液中水的电离判断,离子积常数计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C14H18O5 | B. | C14H16O4 | C. | C16H22O5 | D. | C16H20O5 |
17.某溶液100mL,室温时测得其pH等于1,下列叙述中不正确的是( )
| A. | 该溶液c(H+)≥0.1 mol/L | |
| B. | 把该溶液稀释成1 L后,pH≥2 | |
| C. | 把该溶液稀释成1 L后,pH≤2 | |
| D. | 中和此溶液需0.1mol/L的NaOH体积≥100mL |
11.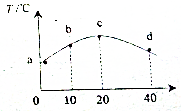 若往20mL 0.01mol•L-1的HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
若往20mL 0.01mol•L-1的HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
 若往20mL 0.01mol•L-1的HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
若往20mL 0.01mol•L-1的HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )| A. | HNO2的电离平衡常数:c点>b点 | |
| B. | 若b点混合溶液显酸性,则2c(Na+)=c(NO2-)+c(HNO2) | |
| C. | c点混合溶液中:c(Na+)>c(OH-)>c(NO2)>c(H+) | |
| D. | d点混合溶液中:c(OH-)=c(HNO2)+c(H+) |
12. C、N、O、Al、Si、Cu是常见的六种元素.
C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元素周期表第三周期第IVA族;
(2)N的基态原子核外电子排布式为1s22s22p3;Cu的基态原子最外层有1个电子;
(3)用“>”或“<”填空:
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动.t1时,原电池中电子流动方向发生改变,其原因是Al在浓硝酸中发生钝化,氧化膜阻止了Al的进一步反应.
 C、N、O、Al、Si、Cu是常见的六种元素.
C、N、O、Al、Si、Cu是常见的六种元素.(1)Si位于元素周期表第三周期第IVA族;
(2)N的基态原子核外电子排布式为1s22s22p3;Cu的基态原子最外层有1个电子;
(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al>Si | N<O | 金刚石>晶体硅 | CH4<SiH4 |
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动.t1时,原电池中电子流动方向发生改变,其原因是Al在浓硝酸中发生钝化,氧化膜阻止了Al的进一步反应.

 ;
;