题目内容
【题目】某化学小组通过查阅资料,设计了如图所示的方法以含镍废催化剂为原料来制备NiSO47H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%). 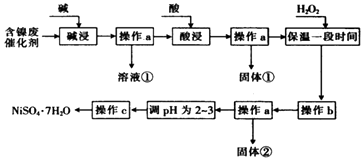
部分阳离子以氢氧化物形式沉淀时的pH如表:
沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
Al(OH)3 | 3.8 | 5.2 |
Fe(OH)3 | 2.7 | 3.2 |
Fe(OH)2 | 7.6 | 9.7 |
Ai(OH)2 | 7.1 | 9.2 |
(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是(填化学式).
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是 .
【答案】
(1)2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑、Al2O3+2OH﹣═2AlO2﹣+3H2O
(2)H2SO4
(3)2Fe2++2H++H2O2=2Fe3++2H2O
(4)3.2≤PH<7.1
【解析】解:(1))“碱浸”过程中是为了除去铝及其氧化物,铝是两性元素和强碱反应,氧化铝是两性氧化物和强碱反应,镍单质和铁及其氧化物不和碱反应达到除去铝元素的目的,反应的离子方程式为:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑、Al2O3+2OH﹣═2AlO2﹣+3H2O,所以答案是:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑、Al2O3+2OH﹣═2AlO2﹣+3H2O;(2)“酸浸”时主要是溶解镍金属和铁单质及其氧化物,依据制备 目的是得到NiSO47H2O,加入的酸不能引入新的杂质,所以需要加入硫酸进行酸浸,
所以答案是:H2SO4;(3)过氧化氢具有强氧化性,可与亚铁离子发生氧化还原反应,反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,
所以答案是:2Fe2++2H++H2O2=2Fe3++2H2O;(4)依据图表中沉淀需要的溶液pH,加入过氧化氢氧化亚铁离子为铁离子后,调节溶液pH使铁离子全部沉淀,镍离子不沉淀得到较纯净的硫酸镍溶液,pH应在3.2﹣7.1间,
所以答案是:3.2≤PH<7.1.

 全优点练单元计划系列答案
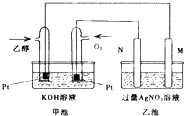
全优点练单元计划系列答案【题目】为验证氧化性:Cl2>Fe3+>SO2 , 某小组用图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如图: 
Ⅰ.打开弹簧夹K1~K4 , 通入一段时间N2 , 再将T型导管插入B中,继续通入N2 , 然后关闭K1、K3、K4 .
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2 .
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3 .
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是 .
(2)棉花中浸润的溶液为 . 作用是
(3)A中发生反应的化学方程式 .
(4)导致步骤Ⅲ中溶液变黄的离子反应是 . 用(写试剂化学式)检验氧化产物,现象是 .
(5)能说明氧化性Fe3+>SO2的离子方程式是 .
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是(填“甲”“乙”“丙”).
过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42﹣ |
乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |