题目内容
5.下列叙述中,正确的是( )| A. | 常温下,pH=3的甲酸溶液的c(H+)与pH=11的氨水溶液中由水电离产生的c(OH-)相等 | |
| B. | 中和 0.1 mol•L-1 醋酸与中和 0.01 mol•L-1的醋酸所需同种碱溶液的物质的量不同 | |
| C. | 向NH4Cl溶液中逐渐加入适量NaOH固体,溶液的导电性明显增强 | |
| D. | 向饱和石灰水中加入少量CaO,恢复至室温后溶液中c(OH-)增大,导电能力增强 |
分析 A.常温下,pH=3的甲酸溶液中c(H+)=10-pHmol/L,pH=11的氨水中的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-pH}}$mol/L;
B.中和不同浓度的醋酸时,所需NaOH物质的量与醋酸的物质的量成正比;
C.NH4Cl溶液中逐渐加入适量NaOH固体生成氯化钠和氨气;
D.饱和溶液的浓度与温度有关.
解答 解:A.常温下,pH=3的甲酸溶液中c(H+)=10-pHmol/L=10-3 mol/L,pH=11的氨水中的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-pH}}$mol/L=10-3 mol/L,故A正确;
B.中和不同浓度的醋酸时,所需NaOH物质的量与醋酸的物质的量成正比,10mL 0.1mol•L-1醋酸与100mL 0.01mol•L-1醋酸的物质的量相等,都是0.001mol,所以中和时需要NaOH的物质的量相等,故B错误;
C.NH4Cl溶液中逐渐加入适量NaOH固体生成氯化钠和氨气,溶液中离子浓度变化不大,所以溶液的导电性变化不大,故C错误;
D.饱和溶液的浓度与温度有关,向饱和石灰水中加入少量CaO,恢复至室温后,温度没有变化,所以仍为饱和溶液,溶液中c(OH-)不变,导电能力不变,故D错误.
故选A.
点评 本题考查弱电解质的电离及溶液pH的有关计算、溶液的导电性等,题目难度不大,注意把握影响饱和溶液浓度的因素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.一定温度下,有式量为M的某物质的饱和溶液V mL,密度为p g•cm-3,该溶液的物质的量浓度为 cmol/L,溶质的质量分数为w,溶液中溶质的质量为mg,此物质在该温度下的溶解度为Sg,则下列表示式中正确的是( )
| A. | m=p•V•w% | B. | w=$\frac{cM}{2000p}$% | C. | S=$\frac{m}{pV-m}$ | D. | c=$\frac{1000m}{VM}$ |
16.下列物质中不能使酸性高锰酸钾溶液褪色的是( )
| A. | CH≡CH | B. | CH2=CH2 | C. | 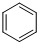 | D. | 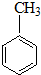 |
13.下列反应的离子方程式正确的是( )
| A. | 用氨水吸收少量的二氧化硫:NH3•H2O+SO2═NH4++HSO3- | |
| B. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O | |
| C. | 次氯酸钙溶液中通入过量的二氧化碳:ClO-+H2O+CO2═HCO3-+HClO | |
| D. | 碳酸钠溶液中慢慢滴入少量稀盐酸:CO32-+2H+═CO2↑+H2O |
17.下列除杂(括号内的为杂质)试剂、方法和相关反应不正确的是( )
| A. | FeCl2(FeCl3)--加入足量铁粉,然后过滤,Fe+2FeCl3═3FeCl2 | |
| B. | NaCl(NaI)--加入适量氯水,用CCl4萃取分液,Cl2+2NaI═2NaCl+I2 | |
| C. | SiO2(Al2O3)--加入足量NaOH溶液,然后过滤,Al2O3+2NaOH═2NaAlO2+H2O | |
| D. | CaCl2(NH4Cl) 固体混合物--直接加热NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑ |
14.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
| A. | CH2=CH2+Br2(CCl4)→ | B. | CH2=CH-CH2-CH3+HCl$→_{△}^{催化剂}$ | ||
| C. | C(CH3)4+Cl2$\stackrel{光照}{→}$ | D. | n CH3-CH=CH2$→_{△}^{催化剂}$ |
15.下列反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | 向漂白粉溶液中加入过量浓盐酸:ClO-+H+=HClO | |
| C. | “万能还原剂”NaBH4与水反应得到NaBO2:BH4-+2H2O=BO2-+4H2↑ | |
| D. | 向FeSO4溶液中加入Na2O2:2Na2O2+2Fe2++2H2O=4Na++2Fe(OH)2↓+O2↑ |
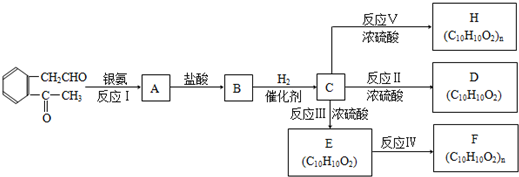
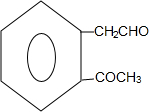 +2Ag(NH3)2OH→
+2Ag(NH3)2OH→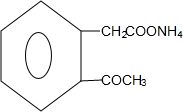 +2Ag↓+3NH3+H2O;
+2Ag↓+3NH3+H2O;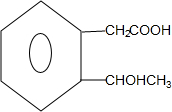 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$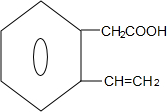 +H2O
+H2O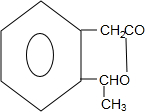 F
F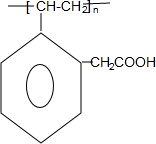 H
H