题目内容
【题目】实验室需要480mL1mol·L-1NaOH溶液,根据溶液配制情况回答下列问题:
(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、玻璃棒外还需要的其他仪器有___。
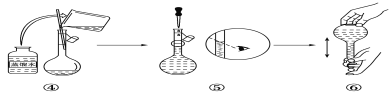
(2)如图是某同学在实验室配制该NaOH溶液的过程示意图,其中有错误的是___(填操作序号)。
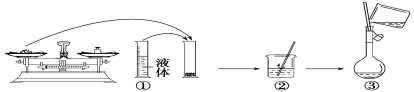
(3)下列操作会导致所配溶液的物质的量浓度偏高的是___。
A.配制NaOH溶液时,NaOH固体中含有Na2O杂质
B.用蒸馏水溶解NaOH固体后,立即转入容量瓶中定容
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出
D.定容时仰视刻度线
E.用托盘天平称量 NaOH 固体时,砝码生锈
F.配制前容量瓶中有少量蒸馏水
(4)若某同学用密度为1.2g/cm3,质量分数为36.5%的浓盐酸配制100mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为___mL。
【答案】胶头滴管、500mL容量瓶 ①③⑤ ABE 25.0
【解析】
(1)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)依据配置一定物质的量浓度溶液的正确操作步骤和仪器的正确使用方法解答;
(3)根据实验操作对![]() 的影响进行误差分析;
的影响进行误差分析;
(4)根据![]() 计算浓度,再根据稀释过程中溶质的物质的量不变,就取浓盐酸的体积。
计算浓度,再根据稀释过程中溶质的物质的量不变,就取浓盐酸的体积。
(1)操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管,根据提供的仪器可知,还需仪器有500ml容量瓶、胶头滴管;
(2)①量筒为量取仪器,不能用来溶解物质,故①错误;
②用玻璃杯搅拌加速固体的溶解,故②正确;
③玻璃棒引流操作时,玻璃棒下端应靠在容量瓶刻度线下方,故③错误;
④加水至刻度线的下方,操作正确,故④正确;
⑤定容时,眼睛应平视刻度线,故⑤错误;
⑥加盖摇匀,使溶液混合均匀,操作正确,故⑥正确;
答案为:①③⑤;
(3)A.配制NaOH溶液时,NaOH固体中含有Na2O杂质,氧化钠和水反应生成NaOH,生成相同物质的量的NaOH,氧化钠需要的质量小,所以会导致NaOH的物质的量偏大,则配制溶液浓度偏大,A符合题意;
B.用水溶解NaOH固体后,立即转入容量瓶中定容,热的溶液体积偏大,冷却后体积变小,则配制的溶液体积偏小,配制的溶液浓度偏高,B符合题意;
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出,配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,C不符合题意;
D.定容时仰视刻度线,导致加入的蒸馏水体积偏大,配制的溶液体积偏多,则配制的溶液浓度偏小,D不符合题意;
E.称量NaOH的固体时,砝码生锈,砝码质量变重,称量的NaOH质量偏大,浓度偏大,E符合题意;
F、容量瓶中有少量蒸馏水,不影响溶质的物质的量和溶液的体积,因此不影响浓度,F不符合题意;
答案选ABE;
(4)浓盐酸的浓度![]() ,配制100mL3mol/L的稀盐酸,根据稀释前后溶质的物质的量不变,设要用量筒量取浓盐酸的体积为VmL,100mL×3mol/L=V×12mol/L,V=25.0mL。
,配制100mL3mol/L的稀盐酸,根据稀释前后溶质的物质的量不变,设要用量筒量取浓盐酸的体积为VmL,100mL×3mol/L=V×12mol/L,V=25.0mL。