题目内容
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物
质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分
含量与时间的关系如图-2所示。下列分析正确的是
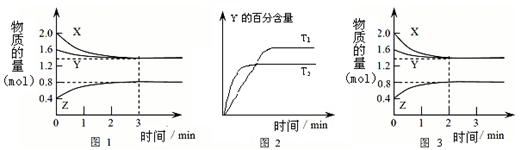
质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分
含量与时间的关系如图-2所示。下列分析正确的是

A.容器中发生的反应可表示为:3X(g)+Y(g) 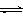 2Z(g) 2Z(g) |
| B.0~3 min内,v(X)=0.2 mol?L-1?min-1 |
| C.其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 |
| D.若改变条件,使反应进程如图-3所示,则改变的条件可能是增大压强 |
AC
试题分析:根据特异性1可知,X,Y的物质的量分别减少了2.0mol-1.4mol=0.6mol、1.6mol-1.4mol=0.2mol。Z的物质的量增加了0.8mol-0.4mol=0.4mol。所以根据变化量之比是相应的化学计量数之比可知,方程式为3X(g)+Y (g)
 2Z(g)。A正确;反应进行的前3 min内,用X表示的反应速率 v(X)=
2Z(g)。A正确;反应进行的前3 min内,用X表示的反应速率 v(X)=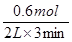 =0.1 mol/(L? min),B错误;根据图像2可知,T1小于T2,温度高,Y的含量低,说明升高温度平衡向正反应方向移动,所以正反应是吸热反应,即△H大于0,重新平衡前v正>v逆 ,C正确;根据图像3可知,平衡状态没有改变,说明改变的条件是加入了催化剂。因为正反应是体积减小的、吸热的可逆反应,所以升高温度或增大压强,平衡都向正反应方向移动,转化率增大,都会改变平衡状态,D错误;
=0.1 mol/(L? min),B错误;根据图像2可知,T1小于T2,温度高,Y的含量低,说明升高温度平衡向正反应方向移动,所以正反应是吸热反应,即△H大于0,重新平衡前v正>v逆 ,C正确;根据图像3可知,平衡状态没有改变,说明改变的条件是加入了催化剂。因为正反应是体积减小的、吸热的可逆反应,所以升高温度或增大压强,平衡都向正反应方向移动,转化率增大,都会改变平衡状态,D错误;
练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
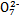 和Cr
和Cr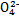 ),其流程为:Cr
),其流程为:Cr Cr2
Cr2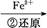 Cr3+
Cr3+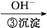 Cr(OH)3↓
Cr(OH)3↓ Cr2
Cr2 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq) Cr2
Cr2 3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是 MgO(s)+CO2(g)+SO2(g) ΔH>0
MgO(s)+CO2(g)+SO2(g) ΔH>0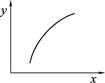
 2C(g) ΔH>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示。则下列说法中,正确的是
2C(g) ΔH>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示。则下列说法中,正确的是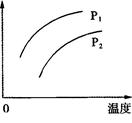
 时,其电离度为0.20(电离度=已电离的HA分子数/起始HA的总分子数);在苯中部分发生双聚,生成(HA)2。该平衡体系中,一元有机弱酸HA在溶剂苯(B)和水(W)中的分配系数为K,K=C(HA)B/C(HA)W=1.0,即达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1;其他信息如下:
时,其电离度为0.20(电离度=已电离的HA分子数/起始HA的总分子数);在苯中部分发生双聚,生成(HA)2。该平衡体系中,一元有机弱酸HA在溶剂苯(B)和水(W)中的分配系数为K,K=C(HA)B/C(HA)W=1.0,即达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1;其他信息如下:
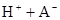

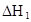
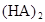
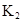
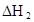
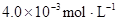
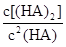 =130,则反应向___________方向进行。
=130,则反应向___________方向进行。 2HI (g)达到平衡的标志是
2HI (g)达到平衡的标志是 CO(NH2)2+H2O,当氨碳比
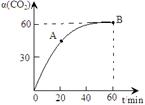
CO(NH2)2+H2O,当氨碳比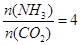 ,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )