题目内容
14.有关物质的转化关系如图所示(部分物质和条件已略去).A、B、D是无色气体,G是红棕色气体,C是年产量最高的金属单质.请回答下列问题: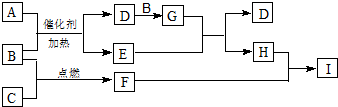
(1)元素B在周期表中的位置为第二周期第ⅥA族.
(2)A的电子式为
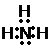 、E的结构式H-O-H、F的化学式为Fe3O4.
、E的结构式H-O-H、F的化学式为Fe3O4.(3)写出A与B反应的化学方程式4NH3+5O2催化剂_△4NO+6H2O.
(4)C单质与过量H的稀溶液反应,也生成I,写出反应的离子方程式Fe+4H++NO3-=Fe3++NO↑+2H2O.
分析 C是年产量最高的金属,则C为Fe,G是红棕色气体,则G为NO2,A、B、D是无色气体,为A与B反应得到D和E,且B与D反应得到NO2,可推知A为NH3、B为O2、D为NO、E为H2O,二氧化氮与水反应生成NO与硝酸,故H为HNO3,Fe在氧气燃烧生成F为Fe3O4,四氧化三铁与硝酸反应生成硝酸铁、氮的氧化物与水,故I为硝酸铁,据此解答.
解答 解:C是年产量最高的金属,则C为Fe,G是红棕色气体,则G为NO2,A、B、D是无色气体,为A与B反应得到D和E,且B与D反应得到NO2,可推知A为NH3、B为O2、D为NO、E为H2O,二氧化氮与水反应生成NO与硝酸,故H为HNO3,Fe在氧气燃烧生成F为Fe3O4,四氧化三铁与硝酸反应生成硝酸铁、氮的氧化物与水,故I为硝酸铁,
(1)由上述分析可知,B为氧气,氧元素位于周期表中的第二周期第ⅥA族,故答案为:第二周期第ⅥA族;
(2)A为NH3,其电子式为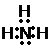
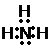
(3)A与B反应是氨气的催化氧化反应生成水与NO,反应的化学方程式为:4NH3+5O2催化剂_△4NO+6H2O
,故答案为:4NH3+5O2催化剂_△4NO+6H2O;
(4)C单质为Fe与过量H为HNO3的稀溶液反应,生成I为硝酸铁,反应的离子方程式为:Fe+4H++NO3-=Fe3++NO↑+2H2O,
故答案为:Fe+4H++NO3-=Fe3++NO↑+2H2O.
点评 本题考查无机物推断,涉及Fe、N元素化合物性质,G的颜色是推断突破口,再结合转化关系进行推断验证,难度不大.

练习册系列答案
相关题目
17.元素在周期表中的位置,能反映原子结构和元素的化学性质,下列有关说法正确的是( )
| A. | 由长、短周期元素共同组成的元素族称为主族 (除零族外) | |
| B. | 同一元素不可能既表现金属性,又表现非金属性 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 互为同位素的不同核素,物理性质和化学性质都不同 |
5.氮氧化物是大气污染物之一,消除氮氧化物的方法有多种.
(1)利用甲烷催化还原氮氧化物.已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
则CH4将NO2还原为N2的热化学方程式为CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol.
(2)利用NH3催化还原氮氧化物的技术叫SCR技术,该技术是目前应用最广泛的烟气氮氧化物脱除技术.反应的化学方程式为2NH3(g)+NO(g)+NO2(g)催化剂_2N2(g)+3H2O(g)△H<0.为提高氮氧化物的转化率可采取的措施是增大NH3的浓度或减小反应体系的压强或降低反应体系的温度等(写出一条即可).
(3)利用ClO2氧化氮氧化物,其转化流程如下:NO→ClO2反应ⅠNO2→Na2SO3反应ⅡN2.已知反应Ⅰ的化学方程式为2NO+ClO2+H2O=NO2+HNO3+HCl,则反应Ⅱ的化学方程式是2NO2+4Na2SO3═N2+4Na2SO4;若生成11.2LN2(标准状况),则消耗ClO267.5g.
(4)用活性碳还原法处理氮氧化物,有关反应为C(s)+2NO(g)?N2(g)+CO2(g)△H,某研究小组向某密闭容器内加入一定量的活性碳和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度下:
①T3℃时,该反应的平衡常数K=0.56(保留两位小数).
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减少CO2浓度.
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H<0(填“>”、“<”或“=”).
(1)利用甲烷催化还原氮氧化物.已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
则CH4将NO2还原为N2的热化学方程式为CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol.
(2)利用NH3催化还原氮氧化物的技术叫SCR技术,该技术是目前应用最广泛的烟气氮氧化物脱除技术.反应的化学方程式为2NH3(g)+NO(g)+NO2(g)催化剂_2N2(g)+3H2O(g)△H<0.为提高氮氧化物的转化率可采取的措施是增大NH3的浓度或减小反应体系的压强或降低反应体系的温度等(写出一条即可).
(3)利用ClO2氧化氮氧化物,其转化流程如下:NO→ClO2反应ⅠNO2→Na2SO3反应ⅡN2.已知反应Ⅰ的化学方程式为2NO+ClO2+H2O=NO2+HNO3+HCl,则反应Ⅱ的化学方程式是2NO2+4Na2SO3═N2+4Na2SO4;若生成11.2LN2(标准状况),则消耗ClO267.5g.
(4)用活性碳还原法处理氮氧化物,有关反应为C(s)+2NO(g)?N2(g)+CO2(g)△H,某研究小组向某密闭容器内加入一定量的活性碳和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度下:
| 浓度/mol.L-1 | NO | N2 | CO2 |
| 时间/min | |||
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.30 | 0.030 |
| 30 | 0.040 | 0.30 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减少CO2浓度.
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H<0(填“>”、“<”或“=”).
9.对于化学反应3W(g)+2X(g)═4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
| A. | v(X)=v(Y) | B. | 3v(W)=2v(X) | C. | 2v(X)=v(Y) | D. | 2v(X)=3v(Z) |
19.已两种气态烃以任意比例混合,在105℃时,1L该混合烃与9L氧气混合,充分燃烧,恢复到原状态,所得气体仍为10L,则这两种烃不可能是( )
| A. | CH4和C2H4 | B. | CH4和C3H6 | C. | C2H4和C3H4 | D. | C2H2和C3H6 |
3.下列各种气体中,其中易液化,遇挥发性酸时冒白烟,而且适宜作致冷剂的是( )
| A. | N2 | B. | NO | C. | NH3 | D. | NO2? |
4.氨是重要的化工原料,可以制尿素等多种产品.
(1)合成氨所用的氢气可以甲烷为原料制得,有关化学反应的能量变化如图1所示.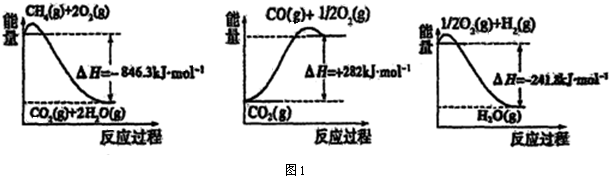
CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为:CH4(g)+H2O(g)=CO(g)+3H2 (g)△H=+161.1kJ•mol-1.
(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合亚铜溶液来吸收原料气中CO,其反应原理为:
[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l);△H<0
吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是B.(填写选项编号)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)?CO(NH2)2(1)+H2O(g)△H<0.某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%.该温度下此反应平衡常数K为2500L2•mol-2.
(4)取两个相同的恒容容器,保持相同温度,并加入等量的CO2气体,根据实验数据绘制出c(NH3)随时间(t)变化的曲线如图2所示,若A、B分别为不同温度时测定的曲线,则A(填“A”或“B”)曲线所对应的实验温度高,判断的依据是A曲线起始浓度小,但在20min时间内反应速率快,说明其温度高.
(5)已知某些弱电解质在水中的电离平衡常数(25℃)如下表:
现有常温下0.1mol•L-1的(NH4)2CO3溶液,
①该溶液呈碱性(填“酸”、“中”、“碱”),原因是由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c(OH-)>c(H+),溶液呈碱性.
②该(NH4)2CO3溶液中各微粒浓度之间的关系式不正确的是B.
A、c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O)
B、c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C、c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D、c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)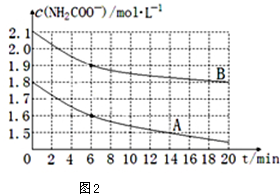
(1)合成氨所用的氢气可以甲烷为原料制得,有关化学反应的能量变化如图1所示.

CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为:CH4(g)+H2O(g)=CO(g)+3H2 (g)△H=+161.1kJ•mol-1.
(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合亚铜溶液来吸收原料气中CO,其反应原理为:
[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l);△H<0
吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是B.(填写选项编号)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)?CO(NH2)2(1)+H2O(g)△H<0.某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%.该温度下此反应平衡常数K为2500L2•mol-2.
(4)取两个相同的恒容容器,保持相同温度,并加入等量的CO2气体,根据实验数据绘制出c(NH3)随时间(t)变化的曲线如图2所示,若A、B分别为不同温度时测定的曲线,则A(填“A”或“B”)曲线所对应的实验温度高,判断的依据是A曲线起始浓度小,但在20min时间内反应速率快,说明其温度高.
(5)已知某些弱电解质在水中的电离平衡常数(25℃)如下表:
| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Kb=1.77×10-5 |
①该溶液呈碱性(填“酸”、“中”、“碱”),原因是由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c(OH-)>c(H+),溶液呈碱性.
②该(NH4)2CO3溶液中各微粒浓度之间的关系式不正确的是B.
A、c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O)
B、c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C、c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D、c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
