题目内容
6.下列溶液中,必须通过焰色反应才能鉴别的一组是( )| A. | Na2CO3 KCl | B. | NaCl KCl | C. | CaCl2 NaCl | D. | K2CO3 CaCl2 |
分析 必须通过焰色反应才能鉴别,则阴离子相同,阳离子为不同活泼金属离子,以此来解答.
解答 解:A.利用盐酸可检验,故A不选;
B.阴离子相同,只能利用焰色反应检验,故B选;
C.阴离子相同,但可利用碳酸钾或碳酸钠检验,故C不选;
D.利用盐酸可检验,故D不选;
故选B.
点评 本题考查物质的鉴别和检验,为高频考点,把握常见离子的检验方法及反应与现象为解答的关键,侧重元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
16.合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A. | 水银 | B. | 青铜 | C. | 生铁 | D. | 碳素钢 |
3.有关碰撞理论,下列说法中不正确的是( )
| A. | 升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大 | |
| B. | 增大反应物浓度,单位体积内活化分子数增多,有效碰撞的几率增大,反应速率增大 | |
| C. | 具有足够能量的分子相互碰撞就一定能发生化学反应 | |
| D. | 正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大 |
11.下列说法错误的是( )
| A. | 微粒半径:S<S2-<K | B. | 稳定性:H2O>H2S>PH3 | ||
| C. | 酸性:H3PO4<HNO3<HClO4 | D. | 沸点:HF<HCl<HBr<HI |
17.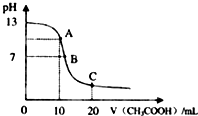 某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
(1)该氢氧化钠溶液的物质的量浓度为0.1mol/L
(2)在A点有关离子浓度大小关系为c(Na+)>c(Ac-)>c(OH-)>c(H+)
(3)配制100mL NaOH标准溶液所需仪器除托盘天平、玻璃棒、胶头滴管、烧杯外,还需要100mL容量瓶
(4)用酸式滴定管量取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定.为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00mL,三次实验结果记录如下:
该盐酸的浓度约为0.109mol.L-1 (保留两位有效数字).滴定达到终点的标志是最后一滴NaOH溶液加入,溶液由无色恰好变成浅红色,半分钟内不褪色
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.碱式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数.
 某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:(1)该氢氧化钠溶液的物质的量浓度为0.1mol/L
(2)在A点有关离子浓度大小关系为c(Na+)>c(Ac-)>c(OH-)>c(H+)
(3)配制100mL NaOH标准溶液所需仪器除托盘天平、玻璃棒、胶头滴管、烧杯外,还需要100mL容量瓶
(4)用酸式滴定管量取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定.为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00mL,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积 | 19.00 | 21.81 | 21.79 |
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.碱式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数.
14.在一可变容积的容器中进行下列反应:H2(g)+I2(g)?2HI(g)达平衡,当温度不变时,增大压强,容器内气体颜色加深,对此正确的说法是( )
| A. | 平衡向生成I2的方向移动 | B. | HI分子减少 | ||
| C. | I2的分子数增多 | D. | I2的浓度增大 |
15.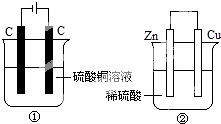 如图两个装置中,分别装有200mL对应的饱和溶液,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,分别装有200mL对应的饱和溶液,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
 如图两个装置中,分别装有200mL对应的饱和溶液,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,分别装有200mL对应的饱和溶液,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A. | 产生气体体积 ①=② | |
| B. | ①中阴极质量增加,②中正极质量减小 | |
| C. | ②中负极:2H++2e-═H2↑ | |
| D. | 溶液的pH变化:①减小,②增大 |
 ;
;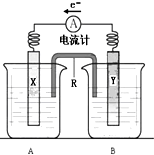 如图是铜锌原电池装置.其电池的总反应是:
如图是铜锌原电池装置.其电池的总反应是: