题目内容
4.下列叙述不正确的是( )| A. | Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | |
| B. | 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入装有足量氯化钡溶液的洗气瓶中(如图装置),洗气瓶中产生的沉淀是硫酸钡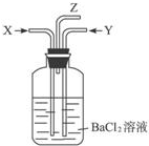 | |
| C. | 向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2 | |
| D. | 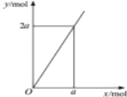 锌与不同浓度的硝酸可发生不同的反应(如图:y表示耗去Zn的物质的量,x表示被还原的硝酸的物质的量),4Zn+10HNO3(极稀)=4Zn(NO3)2+5H2O+N2O↑符合图示 |
分析 A.Ca(ClO)2溶液中通入CO2,生成碳酸钙沉淀和HClO;
B.碳跟浓硫酸共热产生的气体为二氧化碳和二氧化硫,铜跟浓硝酸反应产生的气体为二氧化氮,同时通入装有足量氯化钡溶液发生氧化还原反应生成硫酸钡沉淀;
C.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,反应生成NaHCO3;
D.由图象可知,消耗的锌与被还原的硝酸的物质的量为21,应生成N2O.
解答 解:A.碳酸酸性比次氯酸强,Ca(ClO)2溶液中通入CO2,生成碳酸钙沉淀和HClO,故A正确;
B.碳跟浓硫酸共热产生的气体为二氧化碳和二氧化硫,铜跟浓硝酸反应产生的气体为二氧化氮,同时通入装有足量氯化钡溶液发生氧化还原反应生成硫酸钡沉淀,故B正确;
C.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,反应生成NaHCO3,没有气体生成,故C错误;
D.由图象可知,消耗的锌与被还原的硝酸的物质的量为2:1,则N元素化合价由+5甲应降为+1价,生成N2O,故D正确.
故选C.
点评 本题综合考查元素化合物知识,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意把握物质的性质,难度中等.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
14.下列说法中,不正确的是( )
①同一元素的不同核素互称为同位素
②两个非金属元素原子间不可能形成离子键
③金属腐蚀的实质是金属原子失去电子被还原的过程
④因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
⑤元素的非金属性越强,其氧化物对应的水化物的酸性就越强
⑥青铜、不锈钢、硬铝都是合金
⑦Al和Fe在一定条件下都能与某些氧化物反应
⑧化学键可以使离子相结合,也可以使原子相结合.
①同一元素的不同核素互称为同位素
②两个非金属元素原子间不可能形成离子键
③金属腐蚀的实质是金属原子失去电子被还原的过程
④因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
⑤元素的非金属性越强,其氧化物对应的水化物的酸性就越强
⑥青铜、不锈钢、硬铝都是合金
⑦Al和Fe在一定条件下都能与某些氧化物反应
⑧化学键可以使离子相结合,也可以使原子相结合.
| A. | ③④⑤⑦ | B. | ②⑤⑥⑧ | C. | ①③④⑦ | D. | ③④⑤ |
15.下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和BeCl2 ⑥SiO4-和SO42- ⑦BF3和Al2Cl6.
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和BeCl2 ⑥SiO4-和SO42- ⑦BF3和Al2Cl6.
| A. | 全部 | B. | 除④⑥⑦以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
13.下列图象中的曲线正确的是( )
| A. | 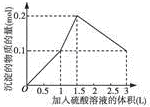 图A表示在1L含0.1mol NaAlO2和0.1mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.11mol•L-1H2SO4溶液,产生沉淀的物质的量与加入硫酸溶液体积的图象 | |
| B. | 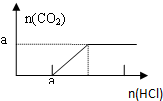 图B表示在分别含amol的Na2CO3和NaOH的混合溶液中逐滴滴加稀盐酸,产生气体 与加入盐酸体积的图象 | |
| C. | 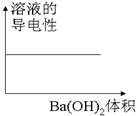 图C表示向100mL 0.1mol/L H2SO4溶液中,逐滴加入0.1mol/L Ba(OH)2溶液至过量, 溶液的导电性与加入 Ba(OH)2溶液体积的图象 | |
| D. | 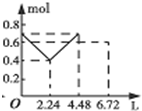 图D表示在往含0.2mol NaOH和0.1mol Ba(OH)2的溶液中持续稳定地通入CO2气体, 溶液中离子数目和通入CO2气体体积的图象(气体的溶解忽略不计) |
14.下列关于晶体的说法正确的是( )
| A. | 熔化二氧化硅和金刚石时所克服的粒子间的作用力类型同种 | |
| B. | 原子晶体的熔点一定比金属的高 | |
| C. | 构成分子晶体的微粒一定含有共价键 | |
| D. | 晶体中只要有阳离子就一定有阴离子 |
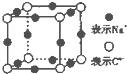 A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A~F为短周期主族元素,G为第四周期元素.已知:A是原子半径最小的元素,B和D同周期,固态的BD2能升华,E、F在B、D的下一周期,且E原子的最外层电子数与次外层电子数之比为3:4;G的质子数比F多12.请回答:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A~F为短周期主族元素,G为第四周期元素.已知:A是原子半径最小的元素,B和D同周期,固态的BD2能升华,E、F在B、D的下一周期,且E原子的最外层电子数与次外层电子数之比为3:4;G的质子数比F多12.请回答: 所示.下列关于有机物 I的说法正确的是CD.
所示.下列关于有机物 I的说法正确的是CD.
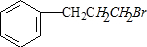 ;
; ;
; +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr.
+NaBr.