题目内容
19.下列属于化学变化的且生成物总能量比反应物总能量高的是( )①液态水汽化;②N2与氧气反应生成NO;③NH4Cl与Ba(OH)2.8H2O反应;④氯酸钾分解制氧气;⑤H2与氧气反应生成H2O.
| A. | ①③④ | B. | ②③④ | C. | ②③ | D. | ③④ |
分析 反应中,生成物总能量比反应物总能量高的反应是吸热反应;
根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:①液态水汽化是物理变化,吸收出大量的热,则属于吸热过程,生成物总能量比反应物总能量高,故①正确;
②N2与氧气反应生成NO为放热反应,在反应中放出热量,故②错误;
③氯化铵与Ba(OH)2•8H20反应是吸热反应,在反应中吸收热量,生成物总能量比反应物总能量高,故③正确;
④氯酸钾分解制氧气为分解反应是吸热反应,在反应中吸收热量,生成物总能量比反应物总能量高,故④正确;
⑤氢气与氧气反应生成H20是常见放热反应,在反应中放出热量,生成物总能量比反应物总能量低,故⑤错误;
故选A.
点评 本题考查吸热反应,明确常见的吸热反应即可解答,掌握基础是解题关键,题目难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
9.下列各种液体分别与溴水混合并振荡,静置后混合液分成两层,下层几乎呈无色的是( )
| A. | 苯 | B. | 己烯 | C. | CCl4 | D. | KI |
10.下列关于Li、Na、K、Rb、Cs的叙述均正确的一组是( )
①金属性最强的是铯
②氧化性最强的是锂离子
③在自然界中均以化合态形式存在
④Li的密度最小
⑤铯与水反应十分剧烈,甚至会发生爆炸
⑥它们的氧化物都只有M2O和M2O2两种形式
⑦粒子半径:Rb+>K+>Na+,Cs>Cs+.
①金属性最强的是铯
②氧化性最强的是锂离子
③在自然界中均以化合态形式存在
④Li的密度最小
⑤铯与水反应十分剧烈,甚至会发生爆炸
⑥它们的氧化物都只有M2O和M2O2两种形式
⑦粒子半径:Rb+>K+>Na+,Cs>Cs+.
| A. | ①②③④ | B. | ④⑤⑥⑦ | C. | ②⑥ | D. | ①②③④⑤⑦ |
7.已知,N2 (g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=92.4 | C. | 2p2<p3 | D. | α1+α2>1 |
4.强碱性溶液中能大量共存的离子组是( )
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、Ag+、Cl-、NO3- | ||
| C. | Ba2+、Na+、NO3-、CO32- | D. | Na+、K+、CO32-、SO32- |
11.Li-SO2电池具有输出功率高和低温性能好等特点.其电解质是LiBr,溶剂是碳酸丙烯酯和乙腈,电池反应为2Li+2SO2$?_{充电}^{放电}$Li2S2O4.下列说法正确的是( )
| A. | 该电池反应为可逆反应 | |
| B. | 放电时,Li+向负极移动 | |
| C. | 充电时,阴极反应式为Li++e-═Li | |
| D. | 该电池的电解质溶液可以换成LiBr的水溶液 |
8.某学生拟用以下厨房用品来区别NaHCO3和NaCl,可行的是( )
| A. | 食醋 | B. | 香油 | C. | 酱油 | D. | 白酒 |
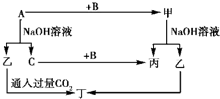 A、B、C是单质,其中A是金属,各种物质间的转化关系如图所示.
A、B、C是单质,其中A是金属,各种物质间的转化关系如图所示.