题目内容
6.2NO2(g)?N2O4(g)达到平衡后下列条件的改变可使NO2气体浓度增大的是( )| A. | 增大容器的容积 | B. | 再充入一定量的N2O4 | ||
| C. | 分离出一定量的NO2 | D. | 再充入一定量的He |
分析 2 NO2=N2O4反应是气体体积减小的放热反应,依据化学平衡原理分析增大二氧化氮浓度的条件.
解答 解:2 NO2=N2O4反应是气体体积减小的放热反应,
A、增大容器体积,各组分浓度均减小,故A错误;
B、再充入四氧化二氮,平衡正向移动,二氧化氮浓度增大,故B正确;
C、减小NO2的浓度,平衡虽逆向进行,二氧化氮的浓度减小,故C错误;
D、体积不变时,再充入一定量的He,总压增大,气体分压不变,平衡不变,二氧化氮浓度不变,故D错误;
故选B.
点评 本题综合综合化学平衡移动的原理以及平衡的影响因素,题目难度中等,注意从等效的角度分析.

练习册系列答案
相关题目
16.液氨与水相似,也存在着微弱的自偶电离:2NH3?NH4++NH2-.对该体系的说法中错误的是( )
| A. | 一定温度下,液氨中c(NH4+)与c(NH2-)的乘积为一常数 | |
| B. | 只要不加入其他物质,液氨中c(NH4+)总是与c(NH2-)相等 | |
| C. | 液氨的电离达到平衡时,c(NH3)=c(NH2-)=c(NH4+) | |
| D. | 液氨中含有NH3、NH4+和NH2- |
1.(1)已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如下表:
则X、Y、Z的电负性从大到小的顺序为Al>Mg>Na(用元素符号表示),元素Y的第一电离能大于X的第一电离能原因是因为元素Mg价电子排布式为3s2完全充满状态,比Al稳定.
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小.D能分别与A、B、C形成XYn型的电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化.
①A、B、C的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
②M是含有极性键(填“极性”或“非极性”)的非极性分子(填“极性”或“非极性”).
③N是一种易液化的气体,请简述其易液化的原因氨分子间存在氢键,因而易液化.
④W分子的VSEPR模型的空间构型为四面体形,W分子的空间构型为V形.
⑤AB-离子中和B2分子的π键数目比为1:1.
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1.
①F元素在其化合物中最高化合价为+6.
②G2+离子的核外电子排布式为1s22s22p63s23p63d9,G2+和N分子形成的配离子的结构式为 .
.
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1 817 | 2 745 | 11 578 |
| Y | 738 | 1 451 | 7 733 | 10 540 |
| Z | 496 | 4 562 | 6 912 | 9 543 |
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小.D能分别与A、B、C形成XYn型的电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化.
①A、B、C的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
②M是含有极性键(填“极性”或“非极性”)的非极性分子(填“极性”或“非极性”).
③N是一种易液化的气体,请简述其易液化的原因氨分子间存在氢键,因而易液化.
④W分子的VSEPR模型的空间构型为四面体形,W分子的空间构型为V形.
⑤AB-离子中和B2分子的π键数目比为1:1.
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1.
①F元素在其化合物中最高化合价为+6.
②G2+离子的核外电子排布式为1s22s22p63s23p63d9,G2+和N分子形成的配离子的结构式为
 .
.
11.下列关于元素周期表的叙述,正确的是( )
| A. | ⅡA族中无非金属元素 | |
| B. | 零族的所有元素均满足最外层电子数为8 | |
| C. | 元素周期表中18个纵行对应18个族 | |
| D. | Ⅷ族中所含元素种类最多 |
18.下列热化学方程式正确的是( )
| A. | 甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3KJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃,101kPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ•mol-1 | |
| D. | 25℃,101Kpa时,强酸与强碱的稀溶液发生反应的中和热为57.3kJ•mol-1,硫酸稀溶液与氢氧化钾稀溶液反应的热化学方程式可表示为:H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(1)△H=-114.6kJ•mol-1 |
15.实验室中关于物质的保存方法,错误的是( )
| A. | 氯水保存在棕色瓶中,冷暗处放置 | B. | 漂白粉可以敞口放置在空气中 | ||
| C. | 液氯可以保存在干燥的钢瓶中 | D. | Na在盛煤油的试剂瓶中密封保存 |
16.某元素一种同位素原子的质子数为m,中子数为n,则下述论断正确的是( )
| A. | 这种元素的相对原子质量为m+n | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | 若碳原子质量为Wg,此原子的质量为(m+n)Wg | |
| D. | 核内中子的总质量小于质子的总质量 |
 是环戊烯的结构简式,可进一步简写为
是环戊烯的结构简式,可进一步简写为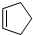 ,环戊烯的化学性质跟链烯烃相似.
,环戊烯的化学性质跟链烯烃相似.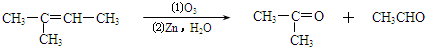
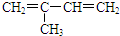 )臭氧化分解各种产物的结构简式及其物质的量之比n(HCHO):n(CH3COCHO)=2:1.
)臭氧化分解各种产物的结构简式及其物质的量之比n(HCHO):n(CH3COCHO)=2:1.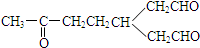 ,A经催化加氢得产物B,B的分子式是C10H20.分析数据表明,分子B内含有六元碳环.则A的键线式为
,A经催化加氢得产物B,B的分子式是C10H20.分析数据表明,分子B内含有六元碳环.则A的键线式为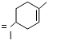 .
.