题目内容
11.下列关于元素周期表的叙述,正确的是( )| A. | ⅡA族中无非金属元素 | |
| B. | 零族的所有元素均满足最外层电子数为8 | |
| C. | 元素周期表中18个纵行对应18个族 | |
| D. | Ⅷ族中所含元素种类最多 |
分析 A.ⅡA族为碱土金属元素;
B.He最外层电子数为2;
C.周期表中有16个族;
D.ⅢB中含錒系和镧系元素.
解答 解:A.ⅡA族为碱土金属元素,则均为金属元素,不含非金属元素,故A正确;
B.He最外层电子数为2,则除He外的零族的所有元素均满足最外层电子数为8,故B错误;
C.周期表中18个纵行、有16个族,故C错误;
D.ⅢB中含錒系和镧系元素,则ⅢB元素种类最多,故D错误;
故选A.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素周期表的周期、族及元素在周期表的位置为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
1. 氮的氧化物的性质、用途和制备受到人们的广泛关注.请回答下列问题.
氮的氧化物的性质、用途和制备受到人们的广泛关注.请回答下列问题.
(1)在恒容密闭容器中,发生反应如下:2N2O5(g)?4NO2(g)+O2(g)△H>0.
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”或“不变”);
②下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率为29.6%;
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1.
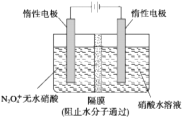
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的阳极区生成,其电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+.
(3)标准状况下,将干燥纯净的NH3和NO2气体分别完成喷泉实验后所得溶液等体积混合,反应后溶液中的离子浓度关系正确的是AC.
A.c(NO3-)>c(NH4+)>c(H+)>c(OH-)
B.c(NH4+)>c(NO3-)>c(OH-)>c(H+)
C.c(H+)=c(OH-)+c(NH3•H2O)
D.c(NH4+)+c(NH3•H2O)=1.5c(NO3-)
 氮的氧化物的性质、用途和制备受到人们的广泛关注.请回答下列问题.
氮的氧化物的性质、用途和制备受到人们的广泛关注.请回答下列问题.(1)在恒容密闭容器中,发生反应如下:2N2O5(g)?4NO2(g)+O2(g)△H>0.
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”或“不变”);
②下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率为29.6%;
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的阳极区生成,其电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+.
(3)标准状况下,将干燥纯净的NH3和NO2气体分别完成喷泉实验后所得溶液等体积混合,反应后溶液中的离子浓度关系正确的是AC.
A.c(NO3-)>c(NH4+)>c(H+)>c(OH-)
B.c(NH4+)>c(NO3-)>c(OH-)>c(H+)
C.c(H+)=c(OH-)+c(NH3•H2O)
D.c(NH4+)+c(NH3•H2O)=1.5c(NO3-)
2.下列说法中正确的是( )
| A. | 因为p轨道是“8”字形的,所以p的电子走“8”字形 | |
| B. | K能级有3s,3p,3d,3f四个轨道 | |
| C. | 氢原子只有一个电子,故氢原子只有一个轨道 | |
| D. | 以上说法均不正确 |
19.第3周期某元素的原子,其最外层3p亚层上有一个未成对电子,则关于该元素的描述正确的是( )
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物水化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
6.2NO2(g)?N2O4(g)达到平衡后下列条件的改变可使NO2气体浓度增大的是( )
| A. | 增大容器的容积 | B. | 再充入一定量的N2O4 | ||
| C. | 分离出一定量的NO2 | D. | 再充入一定量的He |
 ;该微粒还可与Cu2+形成[Cu(H2O)4]+(填化学式)而使CuCl2溶液呈蓝色;
;该微粒还可与Cu2+形成[Cu(H2O)4]+(填化学式)而使CuCl2溶液呈蓝色;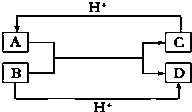
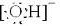 ;C的结构式
;C的结构式 .?
.?